-
(12分)(1)Cu2+能与NH3、Cl-等形成配位数为4的配合物,已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 。
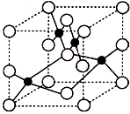
(2)下图是铜的某种氧化物的晶胞结构示意图,该晶体的密度为a g/cm3,设阿伏伽德罗常数的值为NA,则该晶胞的体积为 cm3
(3)0.01mol氯化铬晶体(CrCl3·6H2O)在水溶液中用过量的AgNO3溶液处理,产生0.02molAgCl沉淀,此氯化铬晶体最可能为
a.[Cr(H2O)6] Cl3 b.[Cr(H2O)5 Cl] Cl2·H2O
c.[Cr(H2O)4Cl2] Cl·2H2O d.[Cr(H2O)3Cl3]·3H2O
(4)CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。其中Fe(CO)5常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于
(填晶体类型)。CO与N2 互为等电子体,与CO互为等电子体的离子为 (任写一种);
(5)已知含氧酸可用通式XOm(OH)n来表示,如X是S,当m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m值大的酸性强,m值小的酸性弱。下列各含氧酸中酸性最强的是
a.HClO2 b.H2SeO3 c.H3BO3 d.HMnO4
-
下列说法中错误的是
A.当中心原子的配位数为6时,配合单元常呈八面体空间结构
B.SO3为平面正三角形结构
C.已知[Cu (NH3)2]2+的中心原子采用sp杂化,则它们的空间构型为直线型
D.配位数为4的配合物均为正四面体结构
-
下列说法中错误的是
A.KAl(SO4)2·12H2O不属于配合物
B.配位化合物中的配体可以是分子也可以是阴离子
C.配位数为4的配合物均为正四面体结构
D.已知[Cu(NH3)2]2+的空间构型为直线型,则它的中心原子采用sp杂化
-
Cu2+能与NH3、H2O、C1-等形成配位数为4 的配合物。
(1)[Cu(NH3)4]2+中存在的化学键类型有____(填序号)。
A.配位链 B.极性共价键 C.非极性共价键 D.离子键
(2)[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个C1-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为________________________________。
(3)某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:HOCH2CH=CH2 CH3CH2CHO。在丙烯醇分子中发生某种方式杂化的碳原子数是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原子的杂化方式为____________。
CH3CH2CHO。在丙烯醇分子中发生某种方式杂化的碳原子数是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原子的杂化方式为____________。
-
Cu2+能与NH3、H2O、C1-等形成配位数为4 的配合物。
(1)[Cu(NH3)4]2+中存在的化学键类型有____(填序号)。
A.配位链 B.极性共价键 C.非极性共价键 D.离子键
(2)[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个C1-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为________________________________。
(3)某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:HOCH2CH=CH2 CH3CH2CHO。在丙烯醇分子中发生某种方式杂化的碳原子数是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原子的杂化方式为____________。
CH3CH2CHO。在丙烯醇分子中发生某种方式杂化的碳原子数是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原子的杂化方式为____________。
-
Cu2+能与NH3、H2O、OH﹣、Cl﹣等形成配位数为4的配合物。
(1)向CuSO4溶液中加入过量NaOH溶液可生成Na2[Cu(OH)4]。
①画出配离子[Cu(OH)4]2+中的配位键__。
②Na2[Cu(OH)4]中除了配位键外,还存在的化学键类型有__(填序号)。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2)金属铜单独与氨水或过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液发生如下反应:Cu+H2O2+4NH3═[Cu(OH)4]2++2OH﹣。其原因是_________________.
(3)Cu2+可以与乙二胺(H2N﹣CH2CH2﹣NH2)形成配离子(如图):
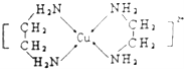
①H、O、N三种元素的电负性从大到小的顺序____。
②乙二胺分子中N原子成键时采取的杂化类型是__。
③乙二胺沸点高于Cl﹣CH2CH2﹣Cl的主要原因是__。
-
Cu2+能与NH3、H2O、OH﹣、Cl﹣等形成配位数为4的配合物。
(1)向CuSO4溶液中加入过量NaOH溶液可生成Na2[Cu(OH)4]。
①画出配离子[Cu(OH)4]2+中的配位键__。
②Na2[Cu(OH)4]中除了配位键外,还存在的化学键类型有__(填序号)。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2)金属铜单独与氨水或过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液发生如下反应:Cu+H2O2+4NH3═[Cu(OH)4]2++2OH﹣。其原因是_________________.
(3)Cu2+可以与乙二胺(H2N﹣CH2CH2﹣NH2)形成配离子(如图):
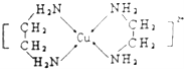
①H、O、N三种元素的电负性从大到小的顺序____。
②乙二胺分子中N原子成键时采取的杂化类型是__。
③乙二胺沸点高于Cl﹣CH2CH2﹣Cl的主要原因是__。
-
Cu2+能与NH3、H2O、OH-、Cl-等形成配位数为4的配合物.
(1)向CuSO4溶液中加入过量NaOH溶液可生成Na2[Cu(OH)4].
①画出配离子[Cu(OH)4]2+中的配位键______.
②Na2[Cu(OH)4]中除了配位键外,还存在的化学键类型有______(填序号).
A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2)金属铜单独与氨水或过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液发生如下反应:
Cu+H2O2+4NH3═[Cu(OH)4]2++2OH-.其原因是______.
(3)Cu2+可以与乙二胺(H2N-CH2CH2-NH2)形成配离子(如图)
①H、O、N三种元素的电负性从大到小的顺序______.
②乙二胺分子中N原子成键时采取的杂化类型是______.
③乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是______.

-
下列说法中错误的是( )
A.SiH4的空间构型是正四面体
B.在NH4+和[Cu(NH3)4]2+中都存在配位键
C.原子晶体中原子以共价键结合,具有键能大、硬度大的特性
D.SO2、SO3都是极性分子
-
配位化合物的数量巨大,组成和结构形形色色,丰富多彩。配合物[Cu(NH3)4](OH)2的中心离子、 配体和配位数分别为
A. Cu+ NH3 4 B. Cu2+ NH3 4 C. Cu2+ OH- 2 D. Cu2+ NH3 2



