-
实验室用 KMnO4 与密度为 1.19 g·cm-3,溶质质量分数为 36.5%的 HCl 溶液反应制取氯气,反应方程式为:
2KMnO4 + 16HCl = 2KCl + 2MnCl 2 + 5Cl 2↑ + 8H2O
(1)用双桥线法分析电子转移的方向和数目____________(直接在上述方程式中表示);
(2)氧化剂_____________ 氧化产物________________
(3)若反应中有 0.5 mol 电子转移,被氧化的 HCl 的物质的量是__________ mol;
(4)c(HCl)=_________________________________ ;
高一化学填空题中等难度题查看答案及解析
-
实验室可用氯酸钾与密度为1.19g•cm﹣3,溶质质量分数为36.5%的浓盐酸反应制取氯气。
I.反应方程式如下:___KClO3+ HCl= KCl+ Cl2↑+ H2O
(1)配平方程式,并用双线桥法表示上述反应中电子转移的方向和数目。
(2)若反应中被氧化的盐酸为5mol,则生成的氯气体积为__________(标准状况下)。
II.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。请回答下列问题:
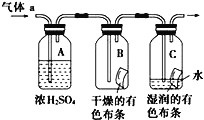
(1)证明氯气和水反应的实验现象为__________,反应的化学方程式是__________。
(2)若将氯气通入石灰乳制取漂白粉,反应的化学方程式是__________,漂白粉溶于水后,遇到空气中的CO2,即产生漂白、杀菌作用,反应的化学方程式是__________。
III.乙同学用上述浓盐酸配置0.100 mol·L-1的稀盐酸480 mL,下列说法正确的是__________。
A.取用240 mL的容量瓶
B.应量取上述浓盐酸的体积为4.2mLC.定容摇匀后发现液面低于刻度线,再加蒸馏水与刻度线相切,所配溶液浓度偏小
D.定容时,仰视刻度线所配溶液浓度偏大
E.量取上述浓盐酸的体积时俯视刻度线所配溶液浓度偏大
高一化学综合题中等难度题查看答案及解析
-
(8分)用KMnO4氧化密度为1.19g·cm-3溶质质量分数为36.5%的HCl溶液。反应方程式如下:
2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O(写出计算过程)
(1)所用HCl溶液的物质的量浓度是多少?
(2)15.8gKMnO4能使多少克HCl发生上述反应?有多少克HCl被氧化?
(3)若Cl2在标准状况下的密度为3.17g·L-1,则产生的Cl2 在标准状况下的体积为多少?
高一化学计算题中等难度题查看答案及解析
-
用KMnO4氧化密度为1.19g/cm3,溶质质量分数为36.5%的盐酸溶液。反应方程式如下:2KMnO4 + 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O
(1)15.8g KMnO4能使多少克HCl发生上述反应?有多少克HCl被氧化?
(2)若Cl 2在标准状况下的密度为3.17g/L,则产生的Cl 2在标准状况下的体积为多少?
高一化学计算题简单题查看答案及解析
-
用KMnO4氧化密度为1.19g•cm-3.溶质质量分数为36.5%的HCl溶液.反应方程式如下:
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法标出上述反应电子转移的方向和数目
(2)15.8gKMnO4能使多少克HCl发生上述反应?有多少克HCl被氧化?
(3)求生成的Cl2 在标准状况下的体积为多少?高一化学解答题中等难度题查看答案及解析
-
用KMnO4氧化密度为1.19g/cm3,溶质质量分数为36.5%的盐酸溶液.反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
(1)15.8g KMnO4能使多少克HCl发生上述反应?有多少克 HCl被氧化?
(2)若Cl2在标准状况下的密度为3.17g/L,则产生的Cl2在标准状况下的体积为多少?高一化学解答题中等难度题查看答案及解析
-
用KMnO4氧化密度为1.19g/cm3,溶质质量分数为36.5%的盐酸溶液.反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
(1)15.8g KMnO4能使多少克HCl发生上述反应?有多少克 HCl被氧化?
(2)若Cl2在标准状况下的密度为3.17g/L,则产生的Cl2在标准状况下的体积为多少?高一化学解答题中等难度题查看答案及解析
-
15.8g KMnO4氧化密度为1.19 g/cm3,溶质质量分数为36.5%的HCl,反应方程式如下:2KMnO4 + 16HCl =2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O。
(1)该盐酸中HCl的物质的量浓度是______________________________。
(2)被氧化的HCl的物质的量为________________________。
(3)求产生的Cl 2在标准状况下的体积(依据化学方程式进行计算,要求写出计算过程)_______。
高一化学计算题简单题查看答案及解析
-
用KMnO4氧化密度为1.19g/cm3,溶质质量分数为36.5%的盐酸。反应方程式如下:
2KMnO4 + 16HCl(浓) = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O
(1)15.8g KMnO4能与________g HCl发生上述反应,其中有________g HCl被氧化。
(2)产生的Cl2在标准状况下的体积为________。
高一化学填空题简单题查看答案及解析
-
(6分)用31.6g KMnO4氧化密度为1.19g/cm3,溶质质量分数为36.5%的盐酸,反应方程式如下:2KMnO4 + 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O
⑴ 该盐酸的物质的量浓度为________?
⑵ 有________mol HCl被氧化?
⑶ 产生的Cl 2在标准状况下的体积为________?
高一化学计算题简单题查看答案及解析