-
工业上利用氨催化氧化法可制取硝酸,加入脱水剂后制得较高浓度的硝酸.以17吨氨作为原料,假设NH3全部转化为HNO3.
(1)写出NH3完全转化为HNO3的总化学反应方程式______
(2)生产过程中需加水吸收,如果与加入脱水剂后脱去水的量相等,则所得硝酸溶液的质量分数为多少?
(3)如果生产中同时制得50%的硝酸m1吨和90%的硝酸m2吨(脱去的水可循环使用,制得较低浓度的稀硝酸),若共加入27吨水,请问m1与m2的质量之比为多少?(要有简单的计算过程)高一化学解答题中等难度题查看答案及解析
-
HNO3是极其重要的化工原料。工业上制备HNO3采用NH3催化氧化法,将中间产生的NO2在密闭容器中多次循环用水吸收制备的。据此完成下列试题:
(1)假如氨制NO的产率是96%,NO制硝酸的产率是92%,氨被硝酸的吸收率为100%,则制备80吨 NH4NO3所需氨的体积(标准状况)为 m3(四舍五入保留整数部分)。
(2)工业上用水吸收二氧化氮生产硝酸,生成的气体经过多次氧化、吸收的循环操作使其充分转化为硝酸(假定上述过程中无其它损失)。
①设循环操作的次数为n,NO2→HNO3转化率与循环操作的次数n之间关系的数学表达式为
②一定量的二氧化氮气体要经过 次循环操作,才能使95%的二氧化氮转变为硝酸。
(3)上述方法制备的HNO3为稀HNO3,将它用水稀释或蒸馏、浓缩可制得不同浓度的HNO3。实验证明:不同浓度的HNO3与同一金属反应可生成不同的还原产物。例如,镁与硝酸反应实验中,测得其气相产物有H2、N2、NO、NO2,液相产物有Mg(NO3)2,NH4NO3和H2O。生成这些产物的HNO3浓度范围为:c(H2)<6.6mol/L、c(N2)<10mol/L、c(NH4+)<10mol/L、0.1mol/L<c(NO)<10mol/L、c(NO2)>0.1mol/L。各气相产物成分及含量随HNO3浓度变化曲线如右图所示。
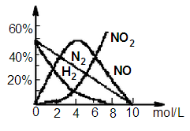
①写出Mg与11mol/L的HNO3反应的化学方程式 。
②960gMg与1000L4mol/L的HNO3恰好完全反应,常温常压下收集到244L气体,试通过计算写出反应方程式 。
高一化学填空题极难题查看答案及解析
-
NH3是重要的化工原料。
(1)工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁。工业上可用氨催化吸收法处理NOx,反应原理为:4x NH3 + 6NOx
(2 x + 3)N2 + 6x H2O
某化学兴趣小组模拟该处理过程的实验装置如下(夹持装置已略去):
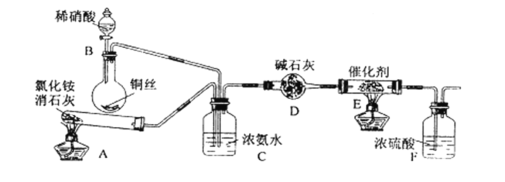
①装置A中发生反应的化学方程式为____________________。
②装置B中发生反应的化学方程式为____________________。
③装置D中碱石灰的作用是__________________________。
(2)按下图装置进行NH3性质实验。
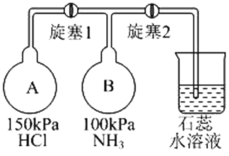
①先打开旋塞1,B瓶中的现象是_________________________________ ,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是_________________ 。
(3)下图是甲同学设计收集氨气的几种装置,其中可行的是________,集气的原理是________。
a.
b.
c.
 d.
d. (4)为防止污染环境,以下装置(盛放的液体均为水)可用于吸收多余氨气的是________(填序号)。
①.
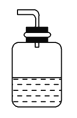 ②.
②. 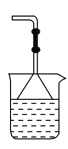 ③.
③.  ④.
④. 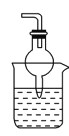
高一化学实验题中等难度题查看答案及解析
-
NH3是重要的化工原料。
(1)工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁。工业上可用氨催化吸收法处理NOx,反应原理为:4xNH3+6NOx
(2x+3)N2+6x H2O
某化学兴趣小组模拟该处理过程的实验装置如下(夹持装置已略去):
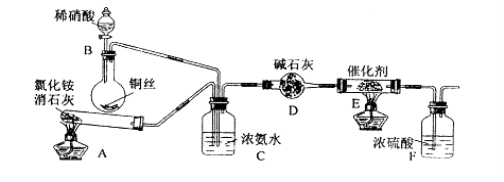
①指出氮氧化物对环境造成的危害 。
②装置A中发生反应的化学方程式为 。
③装置D中碱石灰的作用是 。
(2)按下图装置进行NH3性质实验。

①先打开旋塞1,B瓶中的现象是 ,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是 。
(3)实验室在高温条件下用氨气还原氧化铜的方法测定铜的近似相对原子质量,其产物之一是氮气,写出该反应的化学方程式 。
高一化学实验题困难题查看答案及解析
-
根据所学知识,回答相关问题:
(1)工业上以NH3作为原料制取硝酸,整个过程中涉及三个氧化还原反应,写出这三个氧化还原反应的化学方程式____________、____________、_____________
(2)硫酸具有A−D所示的性质,以下过程主要表现了浓硫酸的那些性质?请将选项字母填在下列各小题的括号内:
A酸性 B吸水性 C脱水性 D强氧化性
①浓硫酸可以干燥氢气______
②浓硫酸使木条变黑______
③热的浓硫酸与铜片反应______
(3)写出足量Al与NaOH溶液反应的离子方程式为_________________,向反应后溶液中通过量CO2的离子方程式为____________________。
高一化学简答题中等难度题查看答案及解析
-
硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_______。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:
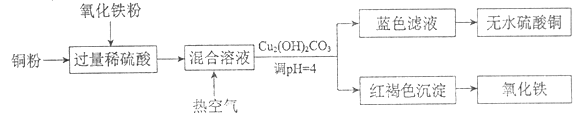
稀硫酸和氧化铁反应的离子方程式是_________;铜和上述反应得到的物质反应的离子方程式是_________;向混合溶液中通入热空气的反应的离子方程式是_________;分离蓝色滤液和红褐色沉淀的实验操作是_________。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:
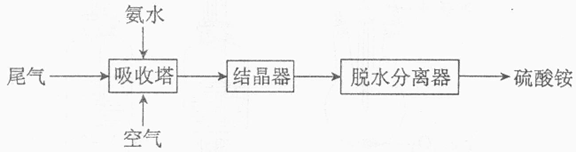
①吸收塔中发生反应的化学方程式是_________。
②检验硫酸铵中的NH4+的离子方程式是_________。
高一化学填空题中等难度题查看答案及解析
-
硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_______。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:
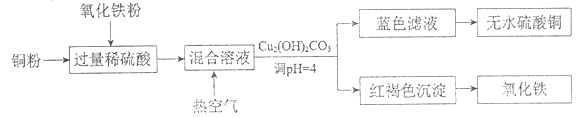
稀硫酸和氧化铁反应的离子方程式是_________;铜和上述反应得到的物质反应的离子方程式是_________;向混合溶液中通入热空气的反应的离子方程式是_________;分离蓝色滤液和红褐色沉淀的实验操作是_________。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:
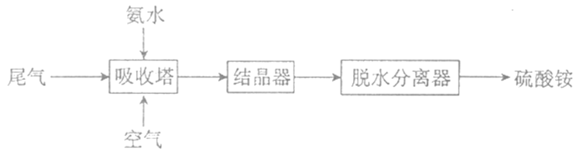
①吸收塔中发生反应的化学方程式是_________。
②检验硫酸铵中的NH4+的离子方程式是_________。
高一化学工业流程中等难度题查看答案及解析
-
(6分)工业上用NH3、氧气和水作原料,合成化肥硝酸铵100 t。
(1)需要NH3________吨,需要氧气________吨。
(2)若NH3制NO转化率为96%,NO制HNO3转化率为92%,需要NH3________吨(保留两位小数)。
【解析】(1)工业生成硝酸铵的反应式为NH3+HNO3=NH4NO3,硝酸铵的物质的量是
,所以根据原子守恒可知需要氨气的物质的量是
,其质量是
,即为42.5吨。其中一半的氨气用来生产硝酸,另一半用来生产硝酸铵。生产硝酸的反应为4NH3+5O2
4NO+6H2O、4NO+3O2+2H2O=4HNO3。即NH3+O2=HNO3+H2O,所以需要氧气的物质的量是
,其质量是
×32g/mol=80×106g,即质量是80吨。
(2)根据(1)的分析可知生产硝酸的理论上需要氨气是21.25吨,所以根据有关转化率可计算,生产硝酸实际需要氨气是
,所以最终需要的氨气是24.06t+21.25t=45.31t。
高一化学计算题简单题查看答案及解析
-
硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_______________________。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:
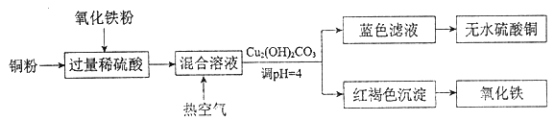
稀硫酸和氧化铁反应的离子方程式是_____________________________;铜和上述反应得到的物质反应的离子方程式是____________________________;向混合溶液中通入热空气的目的是_______________________________;分离蓝色滤液和红褐色沉淀的实验操作是_________。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:
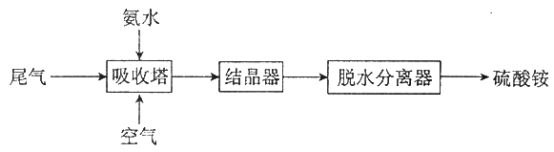
①吸收塔中发生的反应是氧化还原反应,反应中氧化剂和还原剂的物质的量之比是_________。
②检验硫酸铵中的NH4+的离子方程式是_________。
高一化学综合题中等难度题查看答案及解析
-
利用N2→NH3→NO→NO2→HNO3这一过程制备HNO3,有关上述各物质的叙述不正确的是( )
A.工业固氮的常用方法是N2和H2合成NH3
B.可利用Cu与硝酸的反应,将N元素转化为NO或NO2
C.为使上述各步骤依次发生,必须向每个步骤中提供氧化剂
D.实验室可利用氢氧化钙固体与NH4Cl固体混合加热制备NH3高一化学选择题中等难度题查看答案及解析