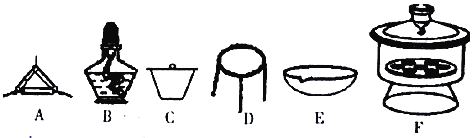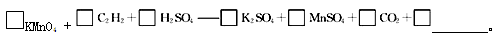-
(9分)为测定碳酸钙纯度(设所含杂质为SiO2),同学们设计了如下两个实验方案:
【方案I】
(1)组装发生并测定生成气体体积的实验装置,并检验气密性;
(2)称取碳酸钙样品W g;
(3)加入过量盐酸;
(4)收集并测定生成的气体体积V mL。
问题I—1:如果称量样品时,砝码底部有一处未被实验者发现的残缺,那么测定的碳酸
钙的纯度会________(填“偏高、偏低、无影响”)。
问题I—2:在方框中画出测定生成的气体体积的装置简图。

【方案II】
(1)称取碳酸钙样品Wg;
(2)在锥形瓶中用C mol/L盐酸V mL(过量)溶解样品;
(3)加入甲基橙作指示剂,再用浓度为C1 mol/L的标准氢氧化钠溶液滴定过量的盐酸,用去氢氧化钠溶液V1毫升。(已知甲基橙的变色范围是pH=3.1~4.4)
问题II—1:未滤去不溶物SiO2,对测定结果是否有影响?(填有或无)________;
理由是________。
问题II—2:碳酸钙纯度表达式________。
【方案评价】
你认为以上两个方案中,最好的方案是,
另一个方案不够好的理由是________。
-
(16分)为测定碳酸钙纯度(设含杂质SiO2),学生设计了如下几个实验方案。请回答每个方案中提出的问题。
【方案I】
(1)称取碳酸钙样品 M g;
(2)加入过量盐酸;
(3)收集并测定生成的气体体积 V mL。
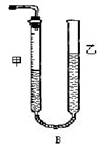
问题1:反应结束后,量气管中的显示如右图所示,接下来的操作是:________,读出甲管中液面的读数。
【方案II】
(1)称取碳酸钙样品 M g;
(2)用c mol/L 盐酸 V mL(过量)溶解样品;
(3)取溶解后的溶液 mL,以酚酞作指示剂,用c′ mol/L NaOH溶液滴定,恰好用去V′mL。
mL,以酚酞作指示剂,用c′ mol/L NaOH溶液滴定,恰好用去V′mL。
问题2:列出本实验中所用到的主要仪器名称(除铁架台及附件、烧杯之外)________。
问题3:碳酸钙纯度计算公式________。
问题4:当碳酸钙溶解完全后,少量未溶的SiO2没过滤去,结果得到碳酸钙纯度________________(偏大、偏小或无影响)
【方案Ⅲ】
(1)称取碳酸钙样品 M g;
(2)加入足量c mol/L盐酸V mL使之完全溶解;
(3)过滤并取滤液;
(4)在滤液中加入过量c′ mol/L Na2CO3溶液V′mL;
(5)将步骤(4)中的沉淀滤出、洗涤、干燥、称重为M′g。
问题5:此方案中不需要的数据是________(填选项编号)。
A.c、V B.c′、 V′ C. M′ D. M
问题6:为减少实验误差,步骤(3)、(5)过滤后都要对沉淀进行洗涤,如果步骤(3)未经洗涤,则测定的碳酸钙的纯度将________(偏大、偏小、无影响,下同);如果步骤(5)未经洗涤,则测定的碳酸钙纯度将________。
问题7:判断步骤(4)中Na2CO3溶液是否过量的方法是________ 。
-
为测定碳酸钙粉末的纯度(含杂质SiO2),某学校学生设计了如下几个实验方案:
方案一:①称取碳酸钙样品M g;②加入过量盐酸;③收集并测定生成的气体体积V mL。
方案二:①称取碳酸钙样品M g;②用c mol/L盐酸V mL(过量)溶解样品;③取溶解后的溶液用c′mol/L NaOH溶液滴定,恰用去V′ mL。
方案三:①称取碳酸钙样品M g;②高温1000 ℃煅烧直至质量不再改变,冷却后称量,质量为M′ g。
方案四:①称取碳酸钙样品M g;②加入足量c mol/L盐酸V mL使之完全溶解;③过滤并取滤液;④在滤液中加入过量的c′mol/L Na2CO3溶液V′mL;⑤将步骤④中的沉淀滤出,洗涤、干燥、称量为M′g。
依据以上实验方案回答以下问题:
(1)方案一中如果称量样品时,砝码底部有一处未被发现的残缺,那么测得的碳酸钙纯度会________(填“偏高”、“偏低”或“无影响”)。
(2)方案二中:列出本实验中所用到的仪器名称(除铁架台、烧杯、铁架台附件外)_________________________________________________________________________。
(3)方案三中的“冷却”应如何操作:
____________________________________________________________;
理由是_________________________________________________________。
(4)方案四中计算碳酸钙纯度的公式为______________;步骤⑤中要将沉淀进行洗涤,如果未经洗涤,则测定结果碳酸钙纯度将________(填“偏高”、“偏低”或“无影响”)。
(5)综上所述,请从实验条件的难易、操作引起实验误差的大小等方面进行综合判断,你认为四个方案中,最好的方案是________。其他方案的缺点分别是:
方案四:沉淀的洗涤、干燥、称量操作过程复杂,容易造成较大误差。
方案________:_____________________________________________________。
方案________:____________________________________________________。
-
(12分)为测定碳酸钙的纯度(设含杂质SiO2),某兴趣小组的同学设计了如下几个实验方案:
方案Ⅰ
①称取碳酸钙样品M g
②用c1mol/L的盐酸V1 mL(过量)溶解样品
③取溶解后的溶液体积的十分之一,用c2 mol/L的NaOH溶液滴定,恰用去V2 mL。
方案Ⅱ
①称取碳酸钙样品M g
②高温煅烧直至质量不再改变,冷却后称量,剩余固体质量为M1 g
方案Ⅲ
①称取碳酸钙样品M g
②加入足量c mol/L的盐酸V mL使之完全溶解
③过滤并取滤液
④在滤液中加入过量c1 mol/L的Na2CO3溶液V1 mL
⑤将步骤④中的沉淀滤出、洗涤、干燥、称重,质量为M1 g。
根据以上实验方案,回答以下问题:
(1)方案Ⅰ中计算碳酸钙纯度的的公式为_________________________________。
(2)方案Ⅱ中的“冷却”应如何操作?________________;理由是_______________________。
(3)方案Ⅲ中不需要的数据是_____________(填选项编号)。
A.c、V B.c1、V1 C.M1 D.M
(4)方案Ⅲ中为了减少实验误差,必要的操作是_______________(填选项编号)。
A.精确测定Na2CO3溶液的体积V1 mL
B.精确配制Na2CO3溶液,使其浓度为c1 mol/L
C.将步骤③所得沉淀洗涤,洗涤液并入④中
(5)请再设计一个实验方案:________________________________。
-
(16分)为测定碳酸钙的纯度(杂质SiO2),学生设计了如下几个实验方案,请回答每个方案中的问题。(相对原子质量:C=12 O=16 Ca=40)
【方案Ⅰ】如图:
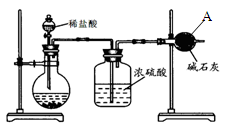
①称取碳酸钙样品m g;
②加入过量盐酸;
③测定仪器A的增重为a g。
(1)仪器A的名称是____________。
【方案Ⅱ】
①称取碳酸钙样品5.0 g;
②用1.00 mol/L盐酸100.0 mL(过量)溶解样品;
③取溶解后溶液体积的1/10 用0.1000mol/L NaOH溶液滴定,重复滴定三次,平均用去15.00mL。
(2)该碳酸钙样品的纯度= 。(计算结果保留三位有效数字)
【方案Ⅲ】
①称取碳酸钙样品mg;
②高温煅烧1000 ℃直至质量不再改变,冷却后称量,固体质量为m’g。
(3)本方案中的“冷却”应在干燥器中进行,理由是 。
【方案Ⅳ】
①称量碳酸钙样品m g;
②加入足量c mol/L盐酸V mL使之完全溶解;
③过滤并取滤液;
④在滤液中加入过量c ’mol/LNa2CO3溶液V’ mL;
⑤将步骤④中的沉淀滤出、洗涤、干燥、称重为b g。
(4)此方案中不需要的数据是(填字母序号) 。
A.m B.c、V C.c’、V’ D.b
(5)综上所述,你认为四个方案中,最好的方案是 。写出其它一个方案的缺点:(如:方案Ⅳ;沉淀的洗涤、干燥、称量操作过程复杂,容易造成较大误差。)
方案 ; 。
-
碱式碳酸镁可用于牙膏、医药化妆品等工业,化学式为4MgCO3·Mg(OH)2·5H2O,某碱式碳酸镁中含有SiO2杂质,为测定其纯度。某兴趣小组设计了如下两个方案:
方案I:
取一定质量的样品,与硫酸充分反应,通过测定CO2的质量计算纯度
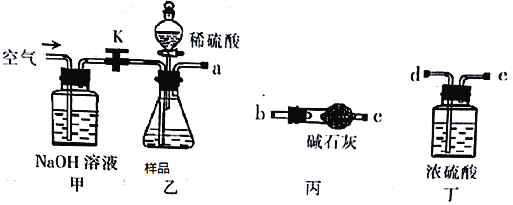
(1)乙中发生反应的方程式为______________________________ 。
(2)仪器接口的连接顺序为(装置可以重复使用) a__________,丁的作用是_________。
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确还应进行的操作是______________________________。
方案Ⅱ:
①称取碱式碳酸镁样品mg;②将样品充分高温灼烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用托盘天平称量)。
(4)下列仪器中,该方案不会用到的是____________。
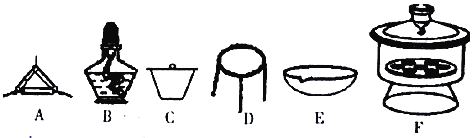
(5)有同学认为方案Ⅱ高温灼烧的过程中会发生MgCO3+SiO2 MgSiO3+CO2↑会导致测定结果有误,你认为这位同学的观点是否正确_____,(填“正确”或“错误”)请说明自己的理由:______________________。
MgSiO3+CO2↑会导致测定结果有误,你认为这位同学的观点是否正确_____,(填“正确”或“错误”)请说明自己的理由:______________________。
-
电石的主要成分为CaC2,易与水反应生成C2H2,故C2H2俗称电石气。某同学设计如下方案测定电石中CaC2的纯度(杂质不参加反应)。

实验原理:CaC2 +2H2O==Ca(OH)2+C2H2 ↑
通过测定生成的气体的体积(标准状况),可确定样品中CaC2的含量。
实验步骤:
①称取样品1.2g;
②把1.2g样品放入气密性良好的气体发生装置,如图所示;
③向样品中滴入水,至不再产生气泡,用量筒排水集气,量筒内液面在360mL处恰与水槽内液面相平;
④作为反应器的烧瓶中有24mL液体。
请回答下列问题:
(1)上述实验所用的玻璃仪器有导管、水槽 、、________、________。
(2)若实验前有1000 mL、500 mL、250 mL的量筒备用,则应选用________ mL的量筒。
(3)生成气体体积是 ________________ mL,为保证生成气体体积的准确性,读取量筒刻度时应注意的问题是________ 。
(4)若将C2H2通入KMnO4溶液中,KMnO4溶液的紫红色会变浅,反应的化学方程式为□KMnO4+□C2H2+□H2SO4——□K2SO4+□MnSO4+□CO2+□________。若该实验生成的 C2H2完全被KMnO4溶液氧化,至少需0.1 mol·L-1的KMnO4溶液________mL。
(5)通过以上数据计算,可得样品中CaC2的纯度为 。
-
(15分)电石的主要成分为CaC2,易与水反应生成C2H2,故C2H2俗称电石气。某同学设计如下方案测定电石中CaC2的纯度(杂质不参加反应)。
实验原理:CaC2+2H2O=Ca(OH)2+C2H2↑
通过测定生成的气体的体积(标准状况),可确定样品中CaC2的含量。
实验步骤:
①取样品1.2g;
②把1.2 g样品放入气密性良好的气体发生装置,如图所示;
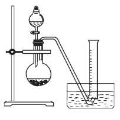
③向样品中滴入水,至不再产生气泡,用量筒排水集气,量筒内液面在360mL处恰与水槽内液面相平
④作为反应器的烧瓶中有24 mL液体。
请回答下列问题:
(1)上述实验所用的玻璃仪器有导管、水槽、 、 、 。
(2)若实验前有1000 mL、500 mL、250 mL的量筒备用,则应选用 mL的量筒。
(3)生成气体体积是 mL,为保证生成气体体积的准确性,读取量筒刻度时应注意的问题是 。
(4)若将C2H2通入KMnO4溶液中,KMnO4溶液的紫红色会变浅,配平并完成化学方程式
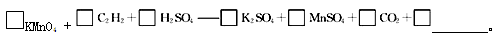
若该实验生成的C2H2完全被KMnO4溶液氧化,至少需0.1 mol • L-1的KMnO4溶液 mL。
(5)通过以上数据计算,可得样品中CaC2的纯度为 。
-
过氧化钠可做航天飞船的供氧剂,对其纯度要求很高,某小组同学为了测定过氧化钠的纯度(杂质为碳酸钠),设计了如下方案:
方案一:取m1g样品,加入 足量的CaCl2溶液,充分反应后过滤、洗涤、干燥,测得CaCO3沉淀质量为m2g;
方案二:取m1g样品,用如下装置测得生成二氧化碳质量为m3g;
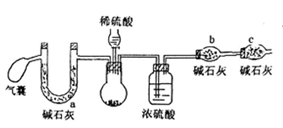
方案三:取m1g样品,加水充分溶解并微热至不再产生气体,用cmol/L的盐酸标准溶液滴定所得溶液(甲基橙作指示剂),终点时消耗盐酸的体积为VmL。
回答下列问题:
(1)方案一中,经正确操作后,测得的过氧化钠的纯度比实际的偏低,其原因是_________;
(2)方案二中气囊要使用两次,第二次使用的目的是__________,C干燥管的作用是_____________,若用稀盐酸代替稀硫酸,则测定结果偏_____(填“高”、“低”或“不影响”)
(3)方案三中,滴定终点的现象是_____________,测得过氧化钠的纯度为_________。(用含m1、c、V的式子表示)
(4)某小组同学向过氧化钠与水反应的溶液中滴加酚酞,发现溶液先变红后褪色,针对导致溶液褪色的原因提出两种假设:
假设一:因氢氧化钠溶液的浓度过大而使溶液褪色
假设二:因生成了过氧化氢而使溶液褪色
实验验证:向等体积浓度分别为5mol•L-1,2mol•L-1,1mol•L-1,0.01mol•L-1的氢氧化钠溶液中滴加酚酞试液,观察到溶液变红后褪色的时间如下:
| 氢氧化钠浓度(mol•L-1) | 5 | 2 | 1 | 0.01 |
| 变红后褪色的时间(s) | 8 | 94 | 450 | 长时间不褪色 |
本实验得出的结论是_____________________________,
设计实验验证假设二_______________________________________________。
-
(12分)有一包含有碳酸钠杂质的碳酸氢钠样品。为了测定其纯度,某校同学在实验室进行如下实验。甲组实验方案:
在坩埚中称取样品3.0g →加热→冷却→称量→再加热•…(至恒重)。
①完成上述实验应该用到的玻璃仪器除酒精灯外还有____ ____。
②若坩埚质量为16.0g,加热至恒重时坩埚和残留物总质量为18.2g,则样品的纯度为_________
(1)乙组:称取样品,利用下面的部分装置测得室温下样品与酸反应放出CO2的体积,计算样品的纯度(已知碳酸钠、碳酸氢钠与酸的反应都是放热反应)。
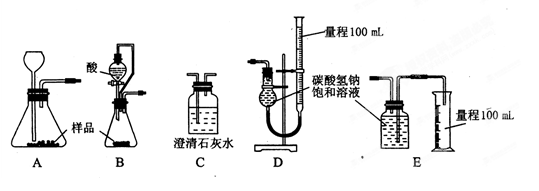
①完成该实验方案应选择的最佳装置是__(用字母回答,下同)。
②该实验应选用的酸是_ _
a.稀盐酸 b.稀硫酸 c.稀硝酸 d.三种酸均可。理由是________________________
(2) 丙组中A同学根据  的反应设计了如下方案:称取样品→配成溶液→加入足量浓CaCl2溶液→充分反应后过滤→洗涤→干燥→称量→计算纯度。
的反应设计了如下方案:称取样品→配成溶液→加入足量浓CaCl2溶液→充分反应后过滤→洗涤→干燥→称量→计算纯度。
B同学对该实验方案提出质疑,丙组同学查阅了相关资料,并进行了如下实验:
室温下,取20 mL0.4 mol/L NaHCO3溶液置于烧杯中,向其中加入20 mL 2 mol/L CaCl2溶液,用玻璃棒搅拌。烧杯中出现白色沉淀,还有气泡产生。产生该现象的原因是_________ __ ___ (用有关离子方程式解释)。
由此丙组同学共同讨论,否定了 A同学的设计方案。