-
化学学习小组对某镁铝合金进行了如下实验研究,请你参与并完成对有关问题的解答.
实验药品:9.0g镁铝合金,100mLa mol/L稀硫酸,260mL5mol/L氢氧化钠溶液.
实验步骤
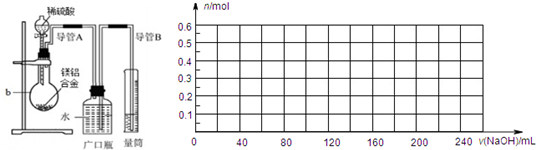
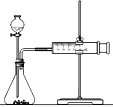
①将9.0g镁铝合金与100mLa mol/L稀硫酸在图所示装置中充分反应至反应完毕,并收集生成的全部气体.
②向b内的混合液中逐滴加入260mL 5mol/L氢氧化钠溶液并充分混合,当氢氧化钠溶液滴加至200mL时生成的沉淀量最大.
问题讨论
(1)仪器b的名称是______.
(2)根据实验目的可知,9.0g镁铝合金与100amol/L稀硫酸反应时,应该过(足)量的物质是______(填“镁铝合金”或“稀硫酸”),以保证另一种物质能够完全反应无剩余.
(3)实验步骤②中,当b内混合液中因滴加氢氧化钠溶液至生成的沉淀量最大时,此时所得溶液中的溶质是______.
(4)实验步骤①结束后,读取量筒所呈现的数据时,需要注意的三个主要问题是:一是要______,二是要调整量筒液面与广口瓶液面相平,三是要使视线与量筒内的凹液面相平.
(5)若标准状况下,由实验步骤①得到的气体体积为10.08L,则合金中镁的质量分数为______.
(6)在“a mol/L稀硫酸”中a的值为______.
(7)请在图中画出实验步骤②中生成沉淀的物质的量(n)随加入氢氧化钠溶液的体积[v(NaOH)]的变化曲线.
-
铝镁合金已成为飞机制造.化工生产等行业的重要材料。研究性学习小组的同学,为测定某含镁3%-5%的镁铝合金(不含其它元素)中镁的质量分数,设计下列如下实验方案进行探究。填写下列空白:
(方案)将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
(1)实验中发生反应的化学方程式是___________________________________________。
(2)用___________称取5.400 g铝镁合金粉末样品,溶于V mL 2.0 mol/L NaOH溶液中,为使其反应完全,则NaOH溶液的体积V≥________mL。
(3)__________、洗涤、__________、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将__________(填“偏高”“偏低”或“无影响”)
-
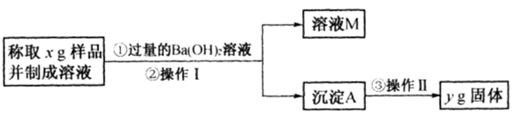
(10分)镁铝合金在交通、航空、电子等行业有着广泛的应用。某化学兴趣小组试对镁铝合金废料进行回收利用,实验中可将铝转化为硫酸铝晶体,并对硫酸铝晶体进行热重分析。镁铝合金废料转化为硫酸铝晶体实验流程如下: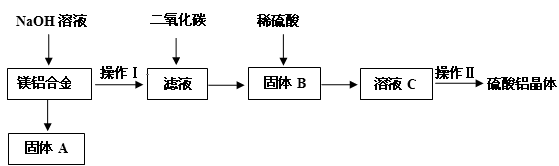
试回答下列问题:
(1)在镁铝合金中加入NaOH溶液,写出反应的化学反应方程式 ,固体B的化学式 。
(2)操作Ⅱ包含的实验步骤有:蒸发浓缩、 、 、洗涤、干燥。
(3)操作Ⅱ中常用无水乙醇对晶体进行洗涤,选用无水乙醇的原因是 。
(4)若初始时称取的镁铝合金废料的质量为9.00 g,得到固体A的质量为4.95 g,硫酸铝晶体的质量为49.95 g(假设每一步的转化率均为100%,合金废料中不含溶于碱的杂质)。计算得硫酸铝晶体的化学式为 。
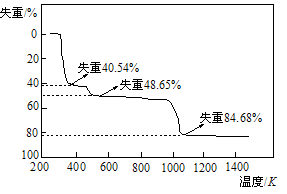
(5)取上述硫酸铝晶体进行热重分析,其热分解主要分为三个阶段:323K-523K,553K-687K,1043K以上不再失重,其热分解的TG曲线见下图,
已知: 。
。
根据图示数据计算确定每步分解的产物,写出第一阶段分解产物的化学式 ,第三阶段反应化学方程式 。
-
化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验,请你参与并完成对有关问题的解答。
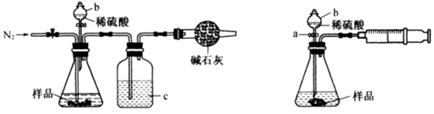
图1 图2
(1)甲同学用图1所示装置测定CO2的质量。实验时稀硫酸是与样品中的________ (填“Na2CO3”或"NaCl”)发生反应。仪器b的名称是________。洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是________ 。
(2)乙同学用图2所示装置,取一定质量的样品(为m g;已测得)和足量稀硫酸反应进行实验,完成样品中Na2CO3”质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的 ________上升,则装置气密性良好。
②在实验完成时,能直接测得的数据是CO2的________ (填“体积’’或“质量’’)。
(3)丙同学用下图所示方法和步骤实验:
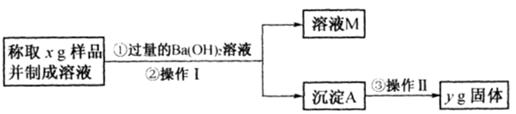
①操作I涉及的实验名称有 ________ 、洗涤;操作Ⅱ涉及的实验名称有干燥、________ 。
②丙测得的样品中Na2CO3质量分数的计算式为________。
(4)标准状况下,将672 mL CO2气通入50 mL1mol/LKOH溶液中,完全反应后,所得溶液中K2CO3和KHCO3的物质的量之比为(设反应前后溶液体积变化忽略不计)________。
-
化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验,请你参与并完成对有关问题的解答。

图1 图2
(1)甲同学用图1所示装置测定CO2的质量。实验时稀硫酸是与样品中的________ (填“Na2CO3”或"NaCl”)发生反应。仪器b的名称是________。洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是________ 。
(2)乙同学用图2所示装置,取一定质量的样品(为m g;已测得)和足量稀硫酸反应进行实验,完成样品中Na2CO3”质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的 ________上升,则装置气密性良好。
②在实验完成时,能直接测得的数据是CO2的________ (填“体积’’或“质量’’)。
(3)丙同学用下图所示方法和步骤实验:
①操作I涉及的实验名称有 ________ 、洗涤;操作Ⅱ涉及的实验名称有干燥、________ 。
②丙测得的样品中Na2CO3质量分数的计算式为________。
(4)标准状况下,将672 mL CO2气通入50 mL1mol/LKOH溶液中,完全反应后,所得溶液中K2CO3和KHCO3的物质的量之比为(设反应前后溶液体积变化忽略不计)________。
-
乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体。某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答。
【观察与思考】
(1)乙醇分子的核磁共振氢谱有 个吸收峰。
【活动与探究】
(2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象。请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满)。
| | 实验现象 | 结 论 |
| ① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
| ② | | |
(3)乙同学向试管中加入3~4 mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,反复多次。则此时乙醇发生反应的化学方程式为(生成乙醛)____________________________________。欲验证此实验的有机产物,可以将产物加入盛有 的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为__________________________________________。
【交流与讨论】
(4)丙同学向一支试管中加入3 mL 乙醇,然后边摇动试管边慢慢加入2 mL浓硫酸和2 mL冰醋酸,按右图所示连接好装置,请指出该装置的主要错误是 。假如乙醇分子中的氧原子为18O原子,则发生此反应后1 8O原子将出现在生成物 中(填字母)。
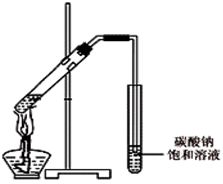
A.水 B.乙酸乙酯 C.水和乙酸乙酯
-
(10分)某化学小组欲以CO2主要为原料,采用下图所示装置模拟“侯氏制碱法”制取NaHCO3,并对CO2与NaOH的反应进行探究。请你参与并完成对有关问题的解答。
【资料获悉】
1、“侯氏制碱法”原理:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,然后再将NaHCO3制成Na2CO3。
2、Na2CO3与盐酸反应是分步进行:Na2CO3先与盐酸反应生成NaHCO3;然后再发生NaHCO3+HCl= NaCl+H2O +CO2↑
【实验设计】

【实验探究】
(1)装置乙的作用是 。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有 、洗涤、灼烧。NaHCO3转化为Na2CO3的化学方程式为 。
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如下图所示。
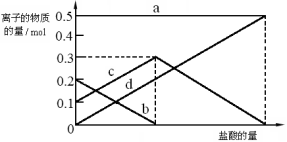
则曲线c对应的溶液中的离子是 (填离子符号);该样品中NaHCO3和Na2CO3的物质的量之比是 。
(4)若将装置甲产生的纯净的CO22.24L(标准状况下)通入100mLNaOH溶液中,充分反应后,将溶液小心蒸干,得到不含结晶水的固体W,其质量为10.16g,则W的成分为 (填化学式),原NaOH溶液的物质的量浓度为 。
-
某化学研究性学习小组对铜及铜的部分化合物的性质进行实验探究,研究的问题和过程如下:
I.氯化铜的制备
该研究性小组在实验室里用下列仪器和药品来制取纯净的无水氯化铜:
图中A、B、C、D、E、F的虚线部分表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白:
(1)如果所制气体从左向右流动时,上述各仪器装置的正确连接顺序是(填各装置的序号)_____接_____接_____接_____接_____接;
(2)装置④的作用是_____________________;
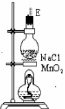
(3)在装置⑤的烧瓶中,发生反应的化学方程式为_____________________;
Ⅱ.探究Cu(OH)2是否和Al(OH)3一样具有两性
(4)该研究性学习小组取适量实验I中制得的产品氯化铜固体充分溶解在一定浓度的盐酸中,过滤,得氯化铜溶液;为探究Cu(OH)2是否和Al(OH)3一样具有两性,除选择配制的CuCl2溶液外,还需要一定选用的试剂为________________;(填序号)
a.氨水 b.氢氧化钠溶液 c.稀硫酸 d.冰醋酸
Ⅲ.为探究不同价态铜的稳定性
(5)该研究性学习小组用实验Ⅱ中所获得的氢氧化铜沉淀制得氧化铜粉末,然后将CuO粉末加热至1000℃以上完全分解成红色的Cu2O粉末,该实验说明:在高温条件下,+l价的Cu比+2价Cu更________(填“稳定”或“不稳定”).
(6)向Cu2O中加适量稀硫酸,得到蓝色溶液和一种红色固体,该反应的离子化学方程式为___________;
-
某化学研究性学习小组对铜及铜的部分化合物的性质进行实验探究,研究的问题和过程如下:
I.氯化铜的制备
该研究性小组在实验室里用下列仪器和药品来制取纯净的无水氯化铜:
图中A、B、C、D、E、F的虚线部分表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白:
(1)如果所制气体从左向右流动时,上述各仪器装置的正确连接顺序是(填各装置的序号)_____接_____接_____接_____接_____接;
(2)装置④的作用是_____________________;
(3)在装置⑤的烧瓶中,发生反应的化学方程式为_____________________;
Ⅱ.探究Cu(OH)2是否和Al(OH)3一样具有两性
(4)该研究性学习小组取适量实验I中制得的产品氯化铜固体充分溶解在一定浓度的盐酸中,过滤,得氯化铜溶液;为探究Cu(OH)2是否和Al(OH)3一样具有两性,除选择配制的CuCl2溶液外,还需要一定选用的试剂为________________;(填序号)
a.氨水 b.氢氧化钠溶液 c.稀硫酸 d.冰醋酸
Ⅲ.为探究不同价态铜的稳定性
(5)该研究性学习小组用实验Ⅱ中所获得的氢氧化铜沉淀制得氧化铜粉末,然后将CuO粉末加热至1000℃以上完全分解成红色的Cu2O粉末,该实验说明:在高温条件下,+l价的Cu比+2价Cu更________(填“稳定”或“不稳定”).
(6)向Cu2O中加适量稀硫酸,得到蓝色溶液和一种红色固体,该反应的离子化学方程式为___________;
-
化学实验是进行化学研究的有效方法,请回答下列实验中的有关问题。
I.用如图所示的装置测定中和热。
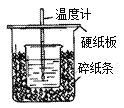
实验药品:100mL 0.50 mol‧L-1盐酸、100mL 0.55 mol‧L-1NaOH溶液。
实验步骤:略。
回答下列问题:
(1)从实验装置上看,还缺少环形玻璃搅拌棒,该装置的作用是____________;有同学提议可以用铜质搅拌棒替代,你是否赞同(说明理由)________________。
(2)你认为该实验成功的关键是______________________________。
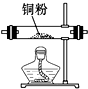
II.影响化学反应速率的因素很多,某校课外兴趣小组用实验的方法进行探究。甲、乙两个兴趣小组利用Mg、Fe、Cu和不同浓度的硫酸(0.5 mol‧L-1、2 mol‧L-1、18.4 mol‧L-1),设计实验方案来研究影响反应速率的因素。
(1)请帮助甲小组完成研究的实验报告:
| 实 验 步 骤 | 现 象 | 结 论 |
| ①分别取等体积0.5 mol‧L-1硫酸于试管中 ②分别投入大小、形状相同的Mg、Fe、Cu ③观察金属表面产生气体的快慢 | ①产生气体的速率Mg>Fe ②Cu上无气体产生 | _________ |
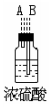
根据控制变量法,要得出正确的实验结论,在实验过程中需要保持温度和压强相同。
(2)乙小组为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验。该小组选用的实验药品是:Fe、2mol‧L-1硫酸和______mol‧L-1硫酸。