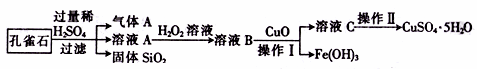-
孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O的步骤如下:

为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下:
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
(1)“除杂”时先通入足量H2O2将Fe2+氧化成Fe3+,再加入CuO固体。其中加入CuO作用是
________,需调节溶液pH的范围为________。
(2)操作X包括 蒸发浓缩、冷却结晶、过滤和洗涤等。在进行该操作时,需要将溶液B再
适当酸化目的________。
(3)若向溶液B中逐滴加入NaOH溶液,刚好出现沉淀时,请写出存在的难溶物质的沉淀溶解平衡方程式为 ________
(4) 为准确测定溶液A中含有Fe2+的物质的量浓度,实验如下:
①取出25.00mL溶液A,配制成250 mL 溶液。
②滴定:准确量取25.00ml所配溶液于锥形瓶中,将0.20mol/LKMnO4溶液
装入________,记录数据。重复滴定2次。平均消耗KMnO4溶液V mL。
(反应式: 5Fe2+ + MnO4— +10 H+ = 5Fe3+ + Mn2+ + 5H2O)
③ 计算溶液A中Fe2+的物质的量浓度=________mol/L (只列出算式,不做运算)。
-
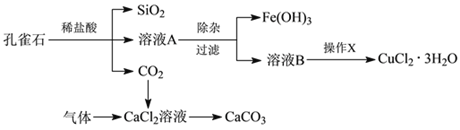
(14分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:
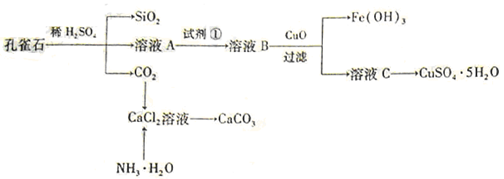
请回答下列问题:(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为 (填代号),检验溶液A中Fe3+的最佳试剂为 (填代号)。
a.KMnO4 b.(NH4) 2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、 、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
(3)由框图可知制备CaCO3时,应向CaCl2溶液中先通入(或先加入) (填化学式)。若实验过程中有氨气逸出,应选用下列 装置回收(填代号)。
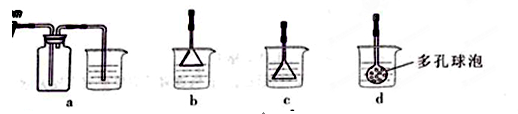
欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时俯视容量瓶的刻度线,会使配制的浓度 。(填“偏高”、“偏低”、“无影响”。)
-
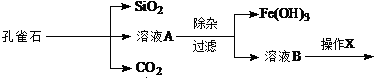
孔雀石的主要成分为Cu2(OH)2CO3,还含少量的FeO、Fe2O3、SiO2。实验室以孔雀石为原料制备CuSO4·5H2O的步骤如下:
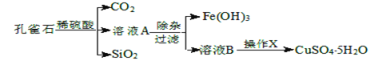
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如表。请回答:
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
(1)孔雀石首先要粉碎,其目的是 _____;溶液A中的金属阳离子有_________;若调pH=9.0将杂质铁元素除去,其后果是:________________________________。
(2)“除杂”时先加入足量H2O2,目的是________________________;再加入CuO固体调节溶液pH的范围至_________,其中加入CuO作用是____________________。
(3)操作X包括________________、_________________、过滤和洗涤等;在进行该操作时,将溶液B再适当酸化目的是_________________________________________。
(4)请设计一种实验方案检验溶液中Fe3+是否完全除去(写出操作步骤、现象和结论)________________。
-
孔雀石的主要成分为Cu2(OH)2CO3,还含少量的FeO、Fe2O3、SiO2。实 验室以孔雀石为
验室以孔雀石为 原料制备CuSO4·5H2O的步骤如下:
原料制备CuSO4·5H2O的步骤如下:
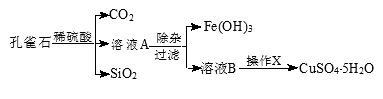
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如右表。请回答:
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
(1)溶液A中的金属阳离子有 ;若调pH=9.0将杂质铁元素除去,其后果是: 。
(2)“除杂”时先加入足量H2O2,目的是 ;再加入CuO固体调节溶液pH的范围至 ,其中加入CuO作用是 。
(3)操作X包括 、 、过滤和洗涤等;在进行该操作时,将溶液B再适当酸化目的是 。
-
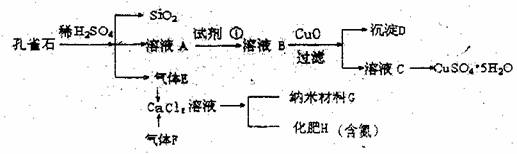
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及纳米材料G,步骤如下:
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①最佳为________(填代号),检验溶液A中Fe3+的最佳试剂为________(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
沉淀D中除了过量的CuO外,还存在另一种固体,其化学式为________。
加入CuO作用是________。
(2)由溶液C获得CuSO4·5H2O,需要经过________操作,
除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是________。
(3)制备纳米材料G时,应向CaCl2溶液中先通入F________(填F的化学式),写出该反应的化学方程式________。
(4)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定(Fe2+被KMnO4氧化), KMnO4标准溶液应用________滴定管,取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,终点现象为________。
(5)下列哪些操作会使测定结果偏高________(填序号)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
-
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,实验室以孔雀石为原料制备CuSO4•5H2O及CaCO3,步骤如下:
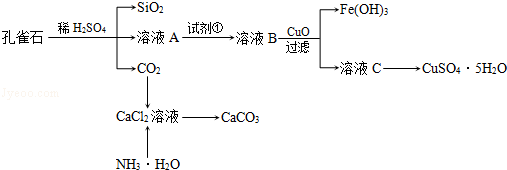
请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+:实验步骤中试剂①为 (从下列所给试剂中选择,填代号),写出此步骤中的离子方程式 ,检验溶液A中Fe3+的最佳试剂为 (从下列所给试剂中选择,填代号).
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4•5H2O,需要经过 、 、过滤等操作.除烧杯、漏斗外,过滤操作还用到另一玻璃仪器 ,该仪器在此操作中的主要作用是 、 .
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入) (填化学式),写出此过程的化学方程式 ,若实验过程中有氨气逸出、应选用下列 装置回收(填代号).
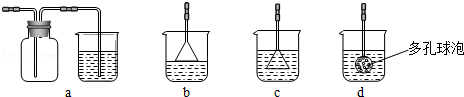
-
(10分)孔雀石的主要成分是CuCO3·Cu(OH)2,还含有少量的SiO2和铁的化合物。实验室以孔雀石为原料制备CuSO4·5H2O的步骤如下:
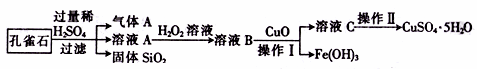
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。若要检验溶液A中Fe2+的最适宜选用的试剂为____ (填代号)。
a.KMnO4 b.铁粉 c.NaCl d.KSCN
(2)向溶液A中加入H2O2的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:_____________________________________________________;实验室选用H2O2而不用Cl2作氧化剂,除考虑环保因素外,另一原因是_____________________________________。
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发,________,过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是________。
(4)将制得的胆矾样品用热重仪进行热重分析,热重仪原理及热重计录如下表:
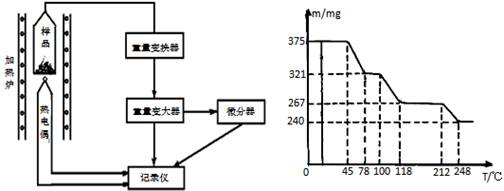
写出212-248℃温度范围内发生反应的化学方程式: 。
-
孔雀石的主要成分是CuCO3•Cu(OH)2,还含有少量的SiO2和铁的化合物.实验室以孔雀石为原料制备CuSO4•5H2O的步骤如下:
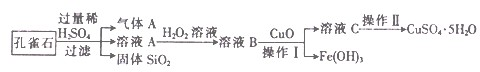
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+.若要检验溶液A中Fe2+的最适宜选用的试剂为______(填代号).
a.KMnO4b.铁粉c.NaCld.KSCN
(2)向溶液A中加入H2O2的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:______;实验室选用H2O2而不用Cl2作氧化剂,除考虑环保因素外,另一原因是______.
(3)由溶液C获得CuSO4•5H2O,需要经过加热蒸发,______,过滤等操作.除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是______.
(4)将制得的胆矾样品用热重仪进行热重分析,热重仪原理及热重计录如下表:
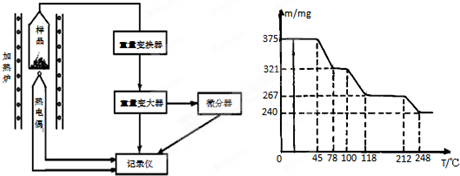
写出212-250℃温度范围内发生反应的化学方程式:______ CuSO4+H2O
-
(12分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。某工厂以孔雀石为主要原料制备 CuSO4·5H2O及纳米材料G,主要步骤如下:

已知该条件下,通过调节溶液的酸碱性而使Fe3+、Fe2+、Cu2 +生成沉淀的pH 分别如下:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |
请回答下列问题:
(1)在相同温度时溶度积的相对大小:Ksp[Fe(OH)2]______(填“>”或“<”)Ksp[Cu(OH)2]。
(2)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。试剂①是一种氧化剂,目的是氧化_____________(填离子符号) 。该工厂选用试剂①最好为下列中的________(填代号)。
a. Na2O2 b. H2O2 c. Cl2 d. KSCN
(3)根据下图有关数据,你认为工业上氧化操作时应采取的措施是溶液温度控制在_______℃,pH控制在________,氧化时间为________小时左右。

(4)向溶液B中加入试剂②的化学式为_______,操作Ⅰ的名称是_________。
(5)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,反应中MnO4-被还原为Mn2+,则该反应的离子方程式为_____________________________________________。取A溶液20.00 mL,用去0.0240 mol/L KMnO4溶液16.00 mL时恰好达到滴定终点,则A溶液中Fe2+浓度为 。
-
(12分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。某工厂以孔雀石为主要原料制备 CuSO4·5H2O及纳米材料G,主要步骤如下:

已知该条件下,通过调节溶液的酸碱性而使Fe3+、Fe2+、Cu2 +生成沉淀的pH 分别如下:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |
请回答下列问题:
(1)在相同温度时溶度积的相对大小:Ksp[Fe(OH)2]______(填“>”或“<”)Ksp[Cu(OH)2]。
(2)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。试剂①是一种氧化剂,目的是氧化_____________(填离子符号) 。该工厂选用试剂①最好为下列中的________(填代号)。
a. Na2O2 b. H2O2 c. Cl2 d. KSCN
(3)根据下图有关数据,你认为工业上氧化操作时应采取的措施是溶液温度控制在_______℃,pH控制在________,氧化时间为________小时左右。
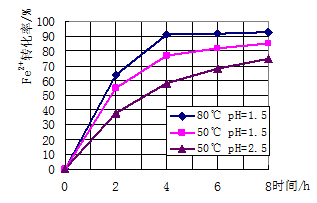
(4)向溶液B中加入试剂②的化学式为_______,操作Ⅰ的名称是_________。
(5)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,反应中MnO4-被还原为Mn2+,则该反应的离子方程式为_____________________________________________。取A溶液20.00 mL,用去0.0240 mol/L KMnO4溶液16.00 mL时恰好达到滴定终点,则A溶液中Fe2+浓度为 。