-
反应:N2(g)+3H2(g) 2NH3(g) △H<0。在等容条件下进行。体系中各物质浓度随时间变化的曲线如图所示,回答问题:
2NH3(g) △H<0。在等容条件下进行。体系中各物质浓度随时间变化的曲线如图所示,回答问题:
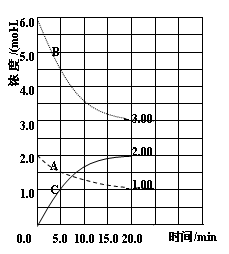
(1)图中B为 (填“N2”、“H2”或“NH3”)计算反应从开始→达平衡时H2的反应速率v(H2)=
(2)下图是在某温度下反应达到平衡,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示体系中各物质的浓度随时间变化的趋势(不需计算新平衡时的具体浓度,只要新平衡时浓度处于一个合理范围内即可。曲线上必须标出N2、H2、NH3)。
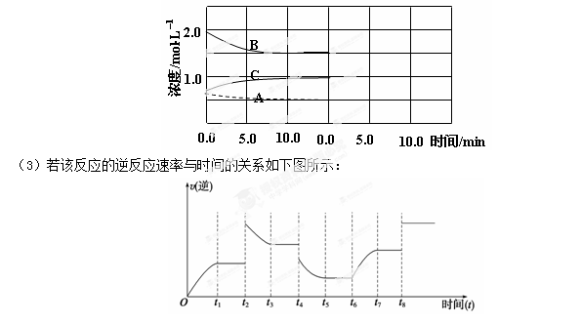
反应在t1、t3、t5、t7时都达到了平衡,而t2、t4、t6、t8时都改变了条件,试判断改变的条件是(填“升温”、“降压”……等);t2时 ;t6时 ;t4时,平衡向 (填“正”或“逆”)反应方向移动。
-
某反应2NH3 N2+3H2在三种不同条件下进行,N2、H2的起始浓度均为0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
N2+3H2在三种不同条件下进行,N2、H2的起始浓度均为0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
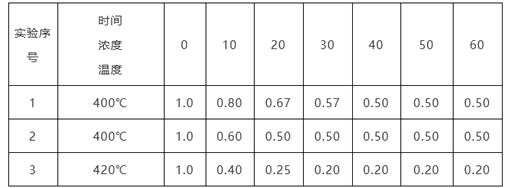
根据上述数据,回答下列问题:
(1)在实验1、2中,有一个实验使用了催化剂,它是______(填字母)。
A.实验1 B.实验2
(2)在实验3中,平衡时NH3的转化率为__________________。
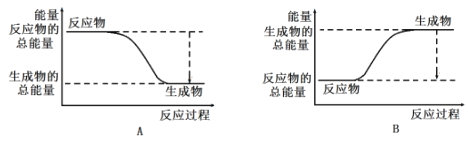
(3)工业合成氨的反应如下:N2+3H2 2NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molNH3中的共价键放出的能量为1173kJ,则由N2和H2生成2molNH3过程中的能量变化为_______kJ。下图能正确表示该反应中能量变化的是______(填字母)。
2NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molNH3中的共价键放出的能量为1173kJ,则由N2和H2生成2molNH3过程中的能量变化为_______kJ。下图能正确表示该反应中能量变化的是______(填字母)。
-
对于可逆反应N2+3H2  2NH3(反应条件略去),回答下列问题:
2NH3(反应条件略去),回答下列问题:
(1)在恒温恒容条件下,下列表述中,不能说明该反应达到平衡状态的有( )
A.体系的压强保持不变
B.某时刻H2和NH3的浓度之比是3:2
C.相同时间内,断裂6NA个N-H键,同时断裂3NA个H-H键
D.某时刻反应速率满足:3v(N2)=v(H2)
E.混合气体的平均摩尔质量不变
(2)下列措施能加快反应速率的有( )
A.降温
B.将NH3分离出体系
C.恒温恒容条件下,加入N2
D.恒温恒压条件下,加入He
(3)若测得达到平衡时,氮气和氢气的转化率相等,则氮气和氢气的起始投料物质的量之比为__________
 (4)若断裂1mol N≡N需要吸热akJ,断裂1molH-H需要吸热bkJ,形成1molN-H放热ckJ, 如果n molN2参加反应(假设N2完全转化),则该过程放热______________kJ
(4)若断裂1mol N≡N需要吸热akJ,断裂1molH-H需要吸热bkJ,形成1molN-H放热ckJ, 如果n molN2参加反应(假设N2完全转化),则该过程放热______________kJ
(5)在恒温恒压的密闭容器中, 加入一定量的氮气和氢气进行反应,若达到平衡时,混合气体的密度是反应前的1.2倍,则达到平衡时,混合气体中氨气的体积分数为_________
-
在容积不变的密闭容器中进行如下反应:N2+3H2  2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是
2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是
①平衡不发生移动;②平衡向正反应方向移动;③平衡向逆反应方向移动;④NH3的质量分数增加;⑤正逆反应速率都增大。
A. ①⑤ B. ③④ C. ②④ D. ②④⑤
-
在2L密闭容器内,t℃时发生反应:N2(g)+3H2(g)⇌2NH3(g),在体系中,n(N2)随时间的变化如下表:
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1)上述反应在第4min时,N2的转化率为___;
(2)用H2表示从0~2min内该反应的平均速率v(H2)=___;
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为__。(用字母填空,下同);
a.v(NH3)=0.04mol·L-1·min-1 b.v(H2)=0.03mol·L-1·min-1
c.v(N2)=0.03mol·L-1·min-1 d.v(H2)=0.00lmol·L-1·s-1
(4)平衡时容器内气体的压强与起始时比__(填“变大”,“变小”或“相等”下同),混合气体的密度与起始时比___。
(5)将amolN2与bmolH2的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(N2)=n(H2)=2n(NH3),则原混合气体中a:b=___。
(6)下列表述能作为反应达到化学平衡状态的标志是__。
a.反应速率v(N2):v(H2):v(NH3)=1:3:2
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内生成nmolN2的同时,生成3nmolH2
f.v(N2)消耗=2v(NH3)消耗
g.单位时间内3molH—H键断裂的同时2molN—H键也断裂
-
在2L密闭容器内,t℃时发生反应:N2(g)+3H2(g) 2NH3(g),在体系中,n(N2)随时间的变化如下表:
2NH3(g),在体系中,n(N2)随时间的变化如下表:
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1)上述反应在第5min时,N2的转化率为___;
(2)用H2表示从0~2min内该反应的平均速率v(H2)=___;
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为___。(用字母填空,下同);
a.v(NH3)=0.05mol·L-1·min-1
b.v(H2)=0.03mol·L-1·min-1
c.v(N2)=0.02mol·L-1·min-1
d.v(H2)=0.00lmol·L-1·s-1
(4)下列表述能作为反应达到化学平衡状态的标志是___。
a.反应速率v(N2)∶v(H2) ∶v(NH3)=1∶3∶2
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
-
在2 L密闭容器内,t℃时发生反应:N2(g)+3H2(g) 2NH3(g),在体系中,n(N2)随时间的变化如下表:
2NH3(g),在体系中,n(N2)随时间的变化如下表:
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1)上述反应在第5min时,N2的转化率为_______________________;
(2)用H2表示从0~2 min内该反应的平均速率v(H2)=_____________;
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为______________。(用字母填空,下同);
a.v(NH3)=0.05 mol·L-1·min-1 b.v(H2)=0.03 mol·L-1·min-1
c.v(N2)=0.02 mol·L-1·min-1 d.v(H2)=0.00 l mol·L-1·s-1
(4)下列表述能作为反应达到化学平衡状态的标志是_____________。
a.反应速率v(N2):v(H2):v(NH3)=1:3:2
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内生成n mol N2的同时,生成3n mol H2
f.v(N2)消耗=2v(NH3)消耗
g.单位时间内3mol H—H键断裂的同时2mol N—H键也断裂
-
一定条件下,某密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g)。反应物N2的浓度
2NH3(g)。反应物N2的浓度
10 s内从2 mol/L降为1 mol/L,在这段时间内用N2浓度的变化表示的反应速率为( )
A.0.05 mol/(L·s) B.0.15 mol/(L·s)
C.0.1 mol/(L·s) D.0.2 mol/(L·s)
-
在一定条件下,对于密闭容器中进行的可逆反应:N2(g) + 3H2(g)  2NH3(g) 。
2NH3(g) 。
下列说法中,表明这一反应已经达到化学平衡状态的是( )
A.N2、H2、NH3的浓度不再变化 B.N2、H2、NH3的浓度相等
C.N2、H2、NH3在密闭容器中共存 D.反应停止,正、逆反应速率都等于零
-
一定条件下,在一体积不变的密闭容器中发生反应:N2(g)+3H2(g)  2NH3(g),能说明该反应达到化学平衡状态的是
2NH3(g),能说明该反应达到化学平衡状态的是
A. N2、H2、NH3的浓度相等
B. 容器内压强不再变化
C. 单位时间内消耗a mol N2,同时生成2a mol NH3
D. 容器内混合气体密度不再变化
2NH3(g) △H<0。在等容条件下进行。体系中各物质浓度随时间变化的曲线如图所示,回答问题:



 2NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molNH3中的共价键放出的能量为1173kJ,则由N2和H2生成2molNH3过程中的能量变化为_______kJ。下图能正确表示该反应中能量变化的是______(填字母)。
2NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molNH3中的共价键放出的能量为1173kJ,则由N2和H2生成2molNH3过程中的能量变化为_______kJ。下图能正确表示该反应中能量变化的是______(填字母)。