| 实验操作 | 时间(min) | 电子天平的读数(g) |
| 烧杯+NaOH溶液 | 120.0 | |
| 烧杯+NaOH溶液+样品 | 135.6 | |
| 1 | 135.1 | |
| 2 | 134.7 | |
| 3 | 134.4 | |
| 4 | 134.4 |
(2)求反应后溶液中的c(OH-)?(假定反应前后溶液体积不变)
(3)若定义:平均反应速率═某物质发生变化的物质的量/反应经历的时间,则用H2物质的量的变化所表示的上述反应从开始到结束时的平均速率为多少?

高一化学解答题中等难度题
| 实验操作 | 时间(min) | 电子天平的读数(g) |
| 烧杯+NaOH溶液 | 120.0 | |
| 烧杯+NaOH溶液+样品 | 135.6 | |
| 1 | 135.1 | |
| 2 | 134.7 | |
| 3 | 134.4 | |
| 4 | 134.4 |

高一化学解答题中等难度题
| 实验操作 | 时间(min) | 电子天平的读数(g) |
| 烧杯+NaOH溶液 | 120.0 | |
| 烧杯+NaOH溶液+样品 | 135.6 | |
| 1 | 135.1 | |
| 2 | 134.7 | |
| 3 | 134.4 | |
| 4 | 134.4 |

高一化学解答题中等难度题查看答案及解析
如图是测定铝粉(含镁粉)的纯度的实验装置。所用的NaOH(足量)的物质的量浓度为4.5 mol·L-1。不同时间电子天平的读数如下表所示:
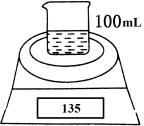
| 实验操作 | 时间/min | 电子天平的读数/g |
| 烧杯+NaOH溶液 | 0 | 120 |
| 烧杯+NaOH溶液+样品 | 0 | 135 |
| 1 | 134.5 | |
| 2 | 134.1 | |
| 3 | 133.8 | |
| 4 | 133.8 |
(1)反应中生成气体的质量 g。
(2)试计算样品中铝的质量分数。(写出解题过程)
(3)反应后溶液(溶液的体积变化忽略)的c(OH-)。(写出解题过程)
高一化学填空题中等难度题查看答案及解析
为了测定小苏打样品的变质情况,取13.7 g固体样品加到100 mL盐酸溶液中,恰好完全反应。产生的气体体积如图所示。请计算
(1)所用盐酸的物质的量浓度。
(2)所取小苏打样品纯度。
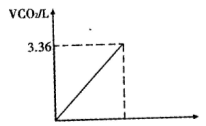
高一化学计算题简单题查看答案及解析
如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置。装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol·L-1。
不同时间电子天平的读数如下表所示:
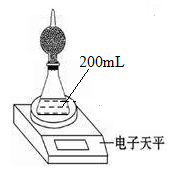
| 实验操作 | t/min | 电子天平的读数/g |
| 装置+硫酸溶液 | 320.0 | |
| 装置+硫酸溶液+样品 | 0 | 335.0 |
| 1 | 334.5 | |
| 2 | 334.1 | |
| 3 | 333.8 | |
| 4 | 333.8 |
(1)反应中生成气体的质量为 。
(2)试计算样品中铝的质量分数?(写出计算过程)
(3)求反应后锥形瓶内硫酸溶液(溶液的体积变化忽略)的物质的量的浓度? (写出计算过程)
高一化学实验题中等难度题查看答案及解析
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。

求:①合金中Mg的质量?
②所用HCl的物质的量浓度?
高一化学计算题中等难度题查看答案及解析
准确称取6.0g铝土矿样品(含Fe2O3),加入100mL稀硫酸中,充分反应后向滤液中加入10mol·L-1NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如图所示。则所用硫酸物质的量浓度为( )
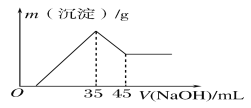
A.1.75mol·L-1 B.3.50mol·L-1
C.0.85mol·L-1 D.无法确定
高一化学单选题中等难度题查看答案及解析
在Na+的物质的量浓度为0.5mol•L-1的某澄清溶液中,还可能含有如下离子:K+、Mg2+、Ba2+、NO3-、CO32-、SO42-。取100mL该溶液进行如下实验(气体体积在标准状况下测定):
I.向该溶液中加入足量稀盐酸,在标准状况下放出0.56L气体(不考虑气体溶解);
II.向I中所得的滤液中滴加足量BaCl2溶液产生白色沉淀2.33g;
下列说法正确的是( )
A.一定不存在的离子是Mg2+、Ba2+,不能确定是否含有K+、NO3-
B.一定存在的离子是CO32-、SO42-,CO32-的物质的量浓度为0.25mol•L-1,SO42-的物质的量浓度为0.1mol•L-1
C.一定存在的离子是CO32-、SO42-、K+,其中K+浓度≥0.2mol•L-1
D.一定存在的离子是CO32-、SO42-、K+,其中K+浓度为0.2mol•L-1
高一化学选择题简单题查看答案及解析
在Na+的物质的量浓度为0.5mol/L的某澄清溶液中,还可能含有如下离子:K+、Mg2+、Ba2+、NO3-、CO32-、SO42-,取100mL 该溶液进行如下实验(气体体积在标准状况下测定):
Ⅰ.向该溶液中加入足量稀盐酸,在标准状况下放出0.56L气体(不考虑气体溶解)
Ⅱ.向Ⅰ中所得的滤液中滴加足量BaCl2溶被产生白色沉淀23.3g;除Na+以外,溶液中离子判断正确的是
A. 只存在的离子是CO32-、SO42-
B. 一定存在的离子是CO32-、SO42-、K+,其中K+浓度≥2mo/L
C. 一定存在的离子是CO32-、SO42-、NO3-,其中NO3-浓度为 0.2mo/L
D. 一定不存在的离子是Mg2+、Ba2+,不能确定是否含有K+、NO3-
高一化学单选题困难题查看答案及解析
工业烧碱中常含有少量NaCl。为测定烧碱中NaOH的质量分数,称取1.6g样品与19.00mL、2.0mol·L—1盐酸恰好反应。
(1)求所消耗盐酸中HCl的物质的量
(2)求工业烧碱中NaOH的纯度
高一化学计算题中等难度题查看答案及解析
实验室进行中和热测定的实验时除需要大烧杯(500 mL)、小烧杯(100 mL)外,所用的其他仪器和试剂均正确的一组是( )
A. 0.50 mol·L-1盐酸,0.50 mol·L-1NaOH溶液,100 mL量筒1个
B. 0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,100 mL量筒2个
C. 0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,50 mL量筒1个
D. 0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,50 mL量筒2个
高一化学单选题中等难度题查看答案及解析