-
根据图示和所学化学键知识回答下列问题:
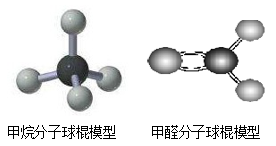
(1)甲醛(CH2O)分子的立体构型为__________,其中碳原子的杂化方式是________。
(2)下列对甲醛分子碳氧键的判断中,正确的是________。
①单键 ②双键 ③极性键 ④非极性键 ⑤σ键 ⑥π键 ⑦σ键和π键 ⑧配位键
(3)下列关于CH4和CO2的说法正确的是_______(填序号)。
a.固态CO2属于分子晶体
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
-
如图是甲醛分子的模型,根据该图和所学化学知识回答下列问题:
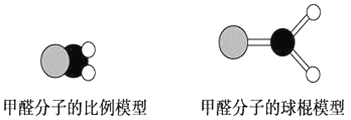
(1)甲醛分子中碳原子的杂化方式是__________,作出该判断的主要理由是__________________________。
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是________(填序号)。
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角________(填“=”、“>”或“<”)120°,出现该现象的主要原因是____________________________________________。
-
如图是甲醛分子的模型,根据该图和所学化学知识回答下列问题:
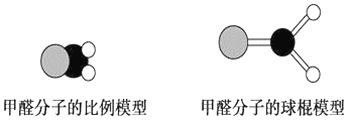
(1)甲醛分子中碳原子的杂化方式是__________,作出该判断的主要理由是__________________________。
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是________(填序号)。
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角________(填“=”、“>”或“<”)120°,出现该现象的主要原因是____________________________________________。
-
如图是甲醛分子的模型,根据该图和所学化学知识回答下列问题:
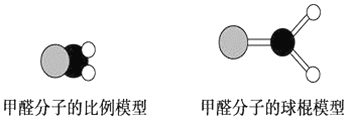
(1)甲醛分子中碳原子的杂化方式是__________,作出该判断的主要理由是__________________________。
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是________(填序号)。
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角________(填“=”、“>”或“<”)120°,出现该现象的主要原因是____________________________________________。
-
下列物质,中心原子的“杂化方式”及“分子空间构型”与CH2O(甲醛)相同的是
A.H2S B.NH3 C.CH2Br2 D.BF3
-
下列物质,中心原子的“杂化方式”及“分子空间构型”与CH2O(甲醛)相同的是
A.H2S B.NH3 C.CH2Br2 D.BF3
-
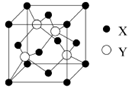
下表为长式周期表的一部分,其中的编号代表对应的元素。
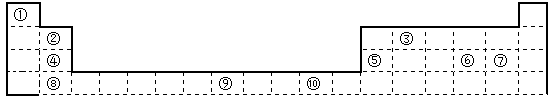
请回答下列问题:
(1)③和①形成的一种5核10电子分子,其立体构型为 ,中心原子杂化方式为 ,属于 分子(填“极性”或“非极性”)。
(2)元素③和⑦的最高价氧化物对应水化物中酸性较强的是: (填化学式)元素⑥的电负性 元素⑦(选填“>”、“=”、“<”=)的电负性。
(3)根据元素周期表分区,元素⑨位于 区,其基态原子电子排布式为 。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的离子方程式 。
-
根据杂化轨道理论和价电子对互斥模型判断,下列分子或者离子的中心原子杂化方式及空间构型正确的是( )
| 选项 | 分子或离子 | 中心原子杂化方式 | 价电子对互斥模型 | 分子或离子的立体构型 |
| A. | SO2 | sp | 直线形 | 直线形 |
| B. | HCHO | sp2 | 平面三角形 | 三角锥形 |
| C. | NF3 | sp2 | 四面体形 | 平面三角形 |
| D. | 
| sp3 | 正四面体形 | 正四面体形 |
A. A B. B C. C D. D
-
根据杂化轨道理论和价电子对互斥模型判断,下列分子或者离子的中心原子杂化方式及空间构型正确的是( )
| 选项 | 分子或离子 | 中心原子杂化方式 | 价电子对互斥模型 | 分子或离子的立体构型 |
| A. | SO2 | sp | 直线形 | 直线形 |
| B. | HCHO | sp2 | 平面三角形 | 三角锥形 |
| C. | NF3 | sp2 | 四面体形 | 平面三角形 |
| D. | 
| sp3 | 正四面体形 | 正四面体形 |
A. A B. B C. C D. D
-
根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的立体构型正确的是( )
| 选项 | 分子式 | 中心原子 杂化方式 | 价层电子对 互斥模型 | 分子或离子 的立体构型 |
| A | SO2 | sp | 直线形 | 直线形 |
| B | HCHO | sp2 | 平面三角形 | 三角锥形 |
| C | NF3 | sp2 | 四面体形 | 平面三角形 |
| D | NH4+ | sp3 | 正四面体形 | 正四面体形 |
A. A B. B C. C D. D





