-
A为短周期元素,A-F6种元素在元素周期表中的位置如图所示,其中A的基态原子的能层序数与最外基电子数相等。回答下列问题(请用元素符号表示相关化学式):

(1)F的价电于排布式为_______________。
(2)B、C、D原子的电负性由大到小的顺序是_______________。
(3)化合物BE2微溶于水,为______(填“极性“成“非极性”)分子,BE2______ (填“能”或“不能”)分离常见的B的单质和正的单质的混合物。
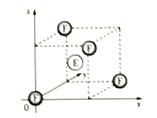
(4)下图为FE晶胞的一部分,F原子的周围最近的E原子有__个;若FE晶胞参数为a,作为数轴单位,在坐标原点的F原于坐标参数记为(0,0,0),则图中E原子的坐标参数为____。
-
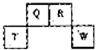
短周期元素Q、R、T、W在元素周期表中位置如图所示,其中T所处的周期序数与主族序数相等,

请回答下列问题:
(1)T的原子结构示意图为 ,R的最简单氢化物的电子式为 ,Q的1:1型氢化物中相对分子质量最小的分子是 型分子(立体构型)。
(2)元素的非金属性为(原子的得电子能力):Q ___________W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为 。
(4)R有多种氧化物,其中氧化物甲的相对分子质量最小。在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是 。
-
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(1)元素的非金属性为(原子的得电子能力):Q______W(填“强于”或“弱于”).可证明此结论的实验事实是______.
(2)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是______ 2H2O+O2↑
-
(12分)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中Q所处的周期序数是其主族序数的一半,请回答下列问题:

 ⑴T的原子结构示意图为_____________。
⑴T的原子结构示意图为_____________。
⑵原子的得电子能力:Q______W(填“强于”或“弱于”)。
 ⑶原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________________________________。
⑶原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________________________________。
⑷W的单质与其最高价氧化物对应的水化物的浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_______________。
 ⑸R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是___________。
⑸R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是___________。
-
I.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示其中Y所处的周期序数与族序数相等。按要求回答下列问题:

(1)写出X的原子结构示意图_______________。
(2)列举一个事实说明X非金属性强于Z: _______________(用化学方程式表示)
(3)含Y的氯化物呈酸性的原因是__________ (用离子方程式表示)
II.运用所学化学原理,解决下列问题:
(4)已知:Si+2NaOH+H2O=Na2SiO3+2H2。某同学利用单质硅和铁为电极材料设计原电池(NaOH为电解质溶液),该原电池负极的电极反应式为_________________;
(5)已知:①C(s)+ O2(g)= CO2(g) H="a" kJ· mol-1;②CO2(g) +C(s)="2CO(g)"
H="a" kJ· mol-1;②CO2(g) +C(s)="2CO(g)" H="b" kJ· mol-1;③Si(s)+ O2(g)=SiO2(s)
H="b" kJ· mol-1;③Si(s)+ O2(g)=SiO2(s) H="c" kJ· mol-1。工业上生产粗硅的热化学方程式_______________________________;
H="c" kJ· mol-1。工业上生产粗硅的热化学方程式_______________________________;
(6)已知:CO(g)+H2O(g) H2(g) + CO2(g)。右上表为该反应在不同温度时的平衡常数。则:该反应的
H2(g) + CO2(g)。右上表为该反应在不同温度时的平衡常数。则:该反应的 H____ 0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为 。
H____ 0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为 。
-
元素A、B、C、D在周期表中的位置如图所示:
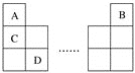
下列叙述中不正确的是( )
A. C的原子序数比B的原子序数大1
B. 原子结构示意图为 的元素,与C位于同一周期
的元素,与C位于同一周期
C. B的原子与D的原子最外层电子数相等
D. 原子结构示意图为 的元素,与B位于同一主族
的元素,与B位于同一主族
-
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子第一至第四电离能如下: I1=738 kJ·mol-1,I2=1451 kJ·mol-1,I3=7733 kJ·mol-1,I4=10540 kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
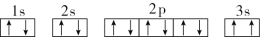 ,该同学所画的电子排布图违背了____________。
,该同学所画的电子排布图违背了____________。
(4)G位于第_____族_____区,该元素的核外电子排布式为_____________________________。
(5)检验F元素的方法是____________。
-
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738 kJ·mol-1 I2=1451 kJ·mol-1 I3=7733 kJ·mol-1 I4=10540 kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:__________________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈_________形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 该同学所画的电子排布图违背了__________________。
该同学所画的电子排布图违背了__________________。
(4)G位于________族________区,该元素的核外电子排布式为_________________。
(5)检验F元素的实验方法是____________,
-
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738 kJ·mol-1 I2=1451 kJ·mol-1 I3=7733 kJ·mol-1 I4=10540 kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中未成对电子最多的元素 |
| G的3d能级只含有2对成对电子 |
(1)已知B2A4是一种无色发烟的、具有腐蚀性和强还原性的无色油状液体,能很好地混溶于水,遇卤素、过氧化氢等强氧化剂作用能自燃。B2A4属于__________分子(填“极性”或“非极性”),B2A4分子中B原子轨道的杂化形式为___________。写出B2A4的电子式:___________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈____形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 该同学所画的电子排布图违背了__________________。
该同学所画的电子排布图违背了__________________。
(4)分析DE3分子的空间构型为__________________。
(5)G位于________族________区,该元素的核外电子排布式为_________________。
(6)无水GE2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水GE2,故常在实验室中用作吸湿剂和空气湿度指示剂。
GE2+xH2O=GE2·xH2O
深蓝色 粉红色
现有65g无水GE2,吸水后变成GE2·xH2O 119g。
①水合物中x=________。
②若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-的个数比为1∶1,则其化学式可表示为 。
-
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738 kJ·mol-1 I2=1451 kJ·mol-1 I3=7733 kJ·mol-1 I4=10540 kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:______________________________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有__________个方向,原子轨道呈_______形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 该同学所画的电子排布图违背___________________。
该同学所画的电子排布图违背___________________。
(4)G位于________族________区,该元素的核外电子排布式为_________________。
(5)DE3中心原子的杂化方式为____________,用价层电子对互斥理论推测其空间构型为__________。
(6)检验F元素的方法是____________,请用原子结构的知识解释产生此现象的原因:_____________。






 ,该同学所画的电子排布图违背了____________。
,该同学所画的电子排布图违背了____________。 该同学所画的电子排布图违背了__________________。
该同学所画的电子排布图违背了__________________。 该同学所画的电子排布图违背了__________________。
该同学所画的电子排布图违背了__________________。 该同学所画的电子排布图违背___________________。
该同学所画的电子排布图违背___________________。