-
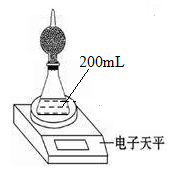
如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置。装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol·L-1。
不同时间电子天平的读数如下表所示:
| 实验操作 | t/min | 电子天平的读数/g |
| 装置+硫酸溶液 | | 320.0 |
| 装置+硫酸溶液+样品 | 0 | 335.0 |
| 1 | 334.5 |
| 2 | 334.1 |
| 3 | 333.8 |
| 4 | 333.8 |
(1)反应中生成气体的质量为 。
(2)试计算样品中铝的质量分数?(写出计算过程)
(3)求反应后锥形瓶内硫酸溶液(溶液的体积变化忽略)的物质的量的浓度? (写出计算过程)
-
某化学兴趣小组研究混有少量氯化钠杂质的纯碱样品,设计如下装置来测定该纯碱样品的纯度。实验步骤如下:
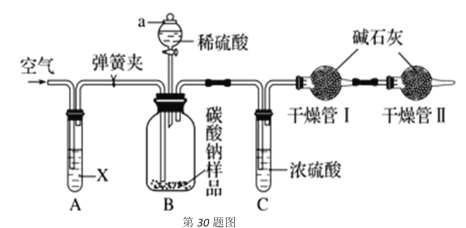
①组装好仪器并检查气密性;
②用托盘天平称量干燥管Ⅰ的质量为m1;
③称量纯碱样品的质量为n,装入广口瓶B内;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤往试管A缓缓鼓入空气数分钟,然后称量干燥管Ⅰ的质量为m2。
请回答:
(1)试剂X是__________,写出广口瓶B中反应的化学方程式__________。
(2)干燥管Ⅱ的作用是__________。
(3)步骤④若滴入稀硫酸过快,会导致测定结果__________(填“偏大”、“偏小”或者“不变”);理由是__________。
(4)根据此实验,计算纯碱样品纯度的为__________(用含m1、m2、n的代数式表示)。
-
某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定该纯碱样品的纯度。实验步骤如下:
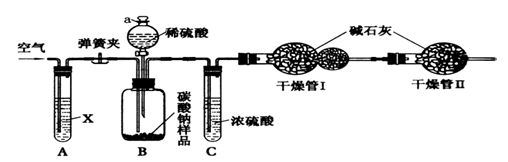
①按图将仪器组装好并检查气密性;②准确称量盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管Ⅰ的质量(设为m1);③准确称量纯碱样品的质量(设为n),放入广口瓶B内;④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;⑤往试管A缓缓鼓入空气数分钟,然后称量干燥管Ⅰ的质量(设为m2)。试回答:
(1)实验操作④、⑤都要缓缓鼓地进行,其理由是_____________,如果这两步操作太快,会导致测定结果________(填偏大、偏小或不变)。
(2)鼓入空气的目的是______________;装置A中的试剂X应选用________________,其作用是__________________,
(3)装置C的作用是___________________;干燥管Ⅱ的作用是__________________。
(4)装置A与B之间的弹簧夹在第_________项操作前必须打开,在第_________项操作用其以前必须夹紧。
(5)根据此实验,写出计算纯碱样品纯度的公式:___________________。
-
如图是测定铝粉(含镁粉)的纯度的实验装置。所用的NaOH(足量)的物质的量浓度为4.5 mol·L-1。不同时间电子天平的读数如下表所示:
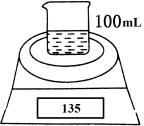
| 实验操作 | 时间/min | 电子天平的读数/g |
| 烧杯+NaOH溶液 | 0 | 120 |
| 烧杯+NaOH溶液+样品 | 0 | 135 |
| 1 | 134.5 |
| 2 | 134.1 |
| 3 | 133.8 |
| 4 | 133.8 |
(1)反应中生成气体的质量 g。
(2)试计算样品中铝的质量分数。(写出解题过程)
(3)反应后溶液(溶液的体积变化忽略)的c(OH-)。(写出解题过程)
-
现有一定量含有Na2O杂质的Na2O2试样,用如图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6mol·L-1盐酸、6mol·L-1硫酸和蒸馏水)
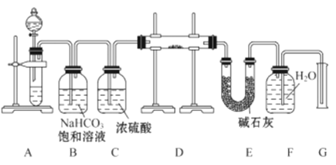
回答下列问题:
(1)装置A中液体试剂选用________
(2)装置B的作用是_________________,装置C的作用是_____________,装置E中碱石灰的作用是______________________________________________。
(3)装置D中发生反应的化学方程式是_________________________。
(4)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为_____________________________________。
-
现有一定量含有Na2O杂质的Na2O2试样,用如图的实验装置测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体、6mo1·L-1盐酸、6mol·L-1硫酸和蒸馏水)。
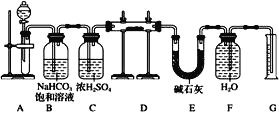
回答下列问题:
(1)装置A中液体试剂选用___。
(2)装置B的作用是___。装置E中碱石灰的作用是___,以及防止水蒸气进入D中干扰实验。
(3)装置D中发生反应的化学方程式是___。
(4)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为___。
-
现有一定量含有Na2O杂质的Na2O2试样,用如图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
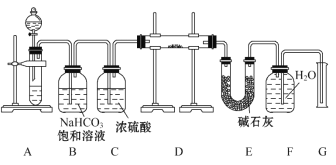
回答下列问题:
(1)装置A中液体试剂选用________
(2)装置B的作用是_________________,装置C的作用是_________________________,装置E中碱石灰的作用是______________________________________________。
(3)装置D中发生反应的化学方程式是_________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为_____________________________________。
-
现有一定量含有Na2O杂质的Na2O2试样,用如图所示实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)回答下列问题:
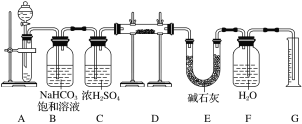
(1)装置A是用来产生CO2气体,则A中液体试剂选用____________,发生反应的离子方程式为___________________。
(2)装置B的作用是_____________________________________________________,装置C的作用是________________________________________________________,装置E中碱石灰的作用是_________________________________________________。
(3)装置D中发生反应的化学方程式为________________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为________。
-
现有一定量含有Na2O杂质的Na2O2试样,用如图所示实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)回答下列问题:
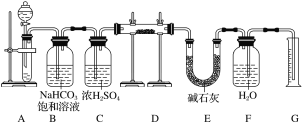
(1)装置A是用来产生CO2气体,则A中液体试剂选用____________,发生反应的离子方程式为___________________。
(2)装置B的作用是_____________________________________________________,装置C的作用是________________________________________________________,装置E中碱石灰的作用是_________________________________________________。
(3)装置D中发生反应的化学方程式为________________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为________。
-
如图所示是测定镁粉(含有少量杂质Al)纯度的实验装置,所用NaOH溶液的浓度为4.5mol/L,体积为100mL,不同时间段电子天平的读数如下表所示:
| 实验操作 | 时间(min) | 电子天平的读数(g) |
| 烧杯+NaOH溶液 | | 120.0 |
| 烧杯+NaOH溶液+样品 | | 135.6 |
| 1 | 135.1 |
| 2 | 134.7 |
| 3 | 134.4 |
| 4 | 134.4 |
(1)请列式计算样品中镁的质量分数?
(2)求反应后溶液中的c(OH-)?(假定反应前后溶液体积不变)
(3)若定义:平均反应速率═某物质发生变化的物质的量/反应经历的时间,则用H2物质的量的变化所表示的上述反应从开始到结束时的平均速率为多少?










