-
(13分)用纯碱和双氧水混合可制作新型液体洗涤剂(2Na2CO3·3H2O2),它具有杀菌消毒去油污的能力且不会污染水源。
(1)捡验这种新型洗涤剂中金属阳离子的操作和现象是 。
(2)这种洗涤剂中的双氧水可以将废水中的CN-转化为无毒物的同时生成NH3,写出该反应的离子方程式 。
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至会完全失去杀菌作用。试分析其中可能的原因(写出其中一种即可,用反应(离子)方程式和简要文字表述) 。
(4)某化学学习小组为了定性探究铁离子对这种新型洗涤剂的不良影响,取该洗涤剂100mL,加入25gFeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0. 1 mol•L-1NaOH溶液、8 mol•L-1 NaOH溶液、澄清石灰水、0.10mol·L-1KMnO4溶液,BaCl2稀溶液、品红溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气休成分提出合理假设。
假设l:气体是O2:。 假设2:气体是CO2。 假设3:气体是
②设计方案:设计实验方案证明假设3,在下表中完成实验步脚、预期现象和结论。

高三化学实验题极难题查看答案及解析
-
用纯碱和双氧水混合可制作新型液体洗涤剂(2Na2CO3·3H2O2),它具有杀菌消毒去油污的能力且不会污染水源。
(1)检验这种新型洗涤剂中金属阳离子的操作和现象是 。
(2)这种洗涤剂中的双氧水可以将废水中的CN一转化生成NH3,写出该反应的离子方程式 。
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至会完全失去杀菌作用。试分析其中可能的原因(写出其中一种即可,用离子方程式和简要文字表述)____________________。
(4)某化学学习小组为了定性探究铁离子对这种新型洗涤剂的不良影响,取该洗涤100mL,加入25gFeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.10mol.L-l NaOH溶液、8.0mol.L-l NaOH:溶液、澄清石灰水、0.l0mol.L-1 KMn04溶液、BaCI2稀溶液、品红溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2。
假设2:气体是CO2。
假设3:气体是
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象和结论。
实验步骤
预期现象和结论
将气体依次通入盛有_____________________、________________的洗气瓶中,并_______________。
___________________________________
高三化学实验题极难题查看答案及解析
-
用纯碱和双氧水混合可制作新型液体洗涤剂(2Na2CO3•3H2O2),它具有杀菌消毒去油污的能力且不会污染水源。
(1)检验这种新型洗涤剂中金属阳离子的操作和现象是______________________;
(2)这种洗涤剂中的双氧水可以将废水中的氰化物转化为无毒物同时生成
,写出反应的离子方程式____________________________;
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至完全失去杀菌作用。试分析其中的原因(写出其中一种即可,用离子方程式和简要文字表述):
__________________________________________________;
(4)某化学学习小组为了定性探究铁离子对这种新型洗涤剂的不良影响,取该洗涤剂100mL,加入25g FeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.10 mol•Lˉ1NaOH溶液、8.0 mol•Lˉ1NaOH溶液、澄清石灰水、0.01 mol•Lˉ1KMnO4溶液、BaCl2稀溶液、品红溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2; 假设2:气体是_____; 假设3:气体是CO2。
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象与结论:
实验步骤
预期现象与结论
将气体依次通入盛有_______、________的洗气瓶中,________________________。
高三化学实验题中等难度题查看答案及解析
-
用纯碱和双氧水混合可制作新型液体洗涤剂(2Na2CO3·3H2O2),它具有杀菌消毒去油污的能力且不会污染水源。
(1)检验这种新型洗涤剂中金属阳离子的操作和现象是_______________________________________。
(2)这种洗涤剂中的双氧水可以将废水中的氰化物转化为无毒物同时生成NH3,写出反应的离子方程式:___________________________________
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至完全失去杀菌作用。试分析其中的原因(用离子方程式和简要文字表述):__________________________________________________________________
(4)某化学学习小组为定性探究铁离子对这种新型洗涤剂的不良影响,取该洗涤剂100 mL,加入25 gFeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.10 mol·L-1 NaOH溶液、8.0 mol·L-1 NaOH溶液、澄清石灰水、0.01 mol·L-1 KMnO4溶液、BaCl2稀溶液、品红溶液、蒸馏水、小木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2;
假设2:气体是________________;
假设3:气体是CO2。
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象与结论。
实验步骤
预期现象与结论
将气体依次通入盛有________、________的洗气瓶中,________
__________________
高三化学实验题困难题查看答案及解析
-
用纯碱和双氧水混合可制作新型液体洗涤剂,它具有杀菌消毒去油污的能力且不会污染水源.
(1)检验这种新型洗涤剂中金属阳离子的操作和现象是________.
(2)这种洗涤剂中的双氧水可以将废水中的氰化物转化为无毒物同时生成NH3,写出反应的离子方程式________
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至完全失去杀菌作用.试分析其中的原因(用离子方程式和简要文字表述)
①________②________
(4)某化学学习小组为了定性探究铁离子对这种新型洗涤剂的不良影响,取该洗涤剂100ml,加入25gFeCl3固体,产生大量无色无味气体,用贮气瓶收集气体.请选用下列试剂和实验用品完成气体成分的探究过程:0.10mol•L-1 NaOH、8.0mol•L-1 NaOH、澄清石灰水、0.01mol•L-1KMnO4、BaCl2稀溶液、品红溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶.
①提出假设:对该气体成分提出合理假设.
假设1:气体是O2;
假设2:气体是________;
假设3:气体是CO2
②设计方案:设计实验方案证明你的假设,在答题卡上完成实验步骤、预期现象与结论:实验步骤 预期现象与结论 将气体依次通入盛有澄清石灰水、________
________的洗气瓶中,________.若澄清石灰水不变浑浊,木条复燃,则假设1成立;
若________,则假设2成立;
若澄清石灰水变浑浊,木条不复燃,则假设3成立.高三化学填空题中等难度题查看答案及解析
-
过碳酸钠(2Na2CO3·3H2O2)是一种新型高效固体漂白杀菌剂,它具有无臭、无毒、无污染的特点,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中。依托纯碱厂制备过碳酸钠可降低生产成本,其生产流程如下:
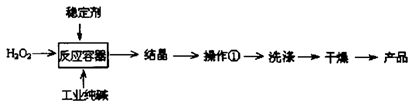
试回答下列问题:
(1)过碳酸钠溶于水后所得溶液一定显________(“酸性”、“碱性”或“中性”)。
(2)操作①需要的玻璃仪器有________(填写仪器名称)。
(3)工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量。
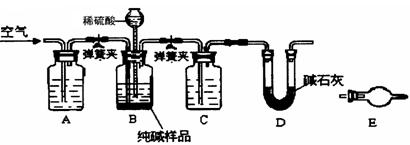
①要检验工业纯碱中杂质的存在,最好选用下列试剂中的(选填序号)。
a.氢氧化钡溶液 b.稀硝酸 c.硫氰化钾溶液 d.硝酸银溶液
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若________,说明
装置不漏气。
③装置A的作用是________,装置C中的试剂为________。
④某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?________
(选填“必要”或“不必要”),判断的理由________。
高三化学填空题中等难度题查看答案及解析
-
过碳酸钠(2Na2CO3·3H2O2)是一种新型高效固体漂白杀菌剂,它具有无臭、无毒、无污染的特点,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中。依托纯碱厂制备过碳酸钠可降低生产成本,其生产流程如下:
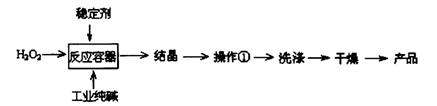
试回答下列问题:
(1)过碳酸钠溶于水后所得溶液一定显________(“酸性”、“碱性”或“中性”)。
(2)操作①需要的玻璃仪器有________(填写仪器名称)。
(3)工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量。
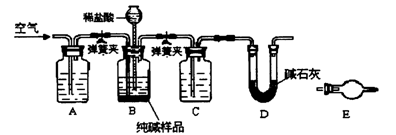
①要检验工业纯碱中杂质的存在,最好选用下列试剂中的________(选填序号)。
a.氢氧化钡溶液 b.稀硝酸 c.硫氰化钾溶液 d.硝酸银溶液
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若________,说明装置不漏气。
③装置A的作用是________,装置C中的试剂为________。
④某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?________
(选填“必要”或“不必要”),判断的理由是________。
高三化学填空题中等难度题查看答案及解析
-
过碳酸钠(2Na2CO4·3H2O)是一种新型高效固体漂白杀菌剂,它具有无臭、无毒、无污染的特点,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中。依托纯碱厂制备过碳酸钠可降低生产成本,其生产流程如下:

试回答下列问题:
(1)过碳酸钠溶于水后所得溶液显________(填“酸性”、“碱性”或“中性”)。请用离子方程式表示:______________________。
(2)操作①需要的玻璃仪器有________(填写仪器名称)。
(3)工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量。

①要检验工业纯碱中杂质的存在,最好选用下列试剂中的__________(选填序号)。
a. 氢氧化钡溶液 b. 稀硝酸 c. 硫氰化钾溶液 d. 硝酸银溶液
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若观察到________说明装置不漏气。
③装置A的作用是,装置C中的试剂为________。
④某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?________(选填“必要”或“不必要”),判断的理由是________。
高三化学实验题极难题查看答案及解析
-
(12分)过碳酸钠(2Na2CO3·3H2O2)俗称固体双氧水,是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的制备流程如下:

(注:BC-1、BC-2均为稳定剂,其中BC-1是由异丙醇和三乙醇胺按一定比例混合而成)
(1)结晶过程中加入氯化钠、搅拌,作用是 。
(2)加入BC-2稳定剂与工业纯碱中含有的Fe3+ 杂质生成稳定的配合物的目的是 。
(3)洗涤抽滤产品,应选用合适的洗涤试剂是 (填写序号)。
A.饱和氯化钠溶液 B.水 C.异丙醇 D.碳酸钠饱和溶液
(4)工业上常以活性氧的质量分数[ω(活性氧)=16 n(H2O2) / m(样品) ×100﹪]来衡量过碳酸钠产品的优劣,ω≥13﹪为优等品。现将0.2000g某厂家生产的过碳酸钠样品(所含杂质不参与后面的反应)溶于水配成溶液,加入适量稀硫酸酸化,再加入足量KI,摇匀后静置于暗处,充分反应后加入少量淀粉试剂,用0.1000mol/LNa2S2O3溶液滴定到终点,消耗Na2S2O3溶液33.00mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI),通过计算判断样品是否为优等品(写出计算过程)。
高三化学填空题困难题查看答案及解析
-
4Na2SO4•2H2O2•NaCl又称固体双氧水,具有漂白、杀菌、消毒作用,又由于其稳定性比过碳酸钠(2Na2CO3•3H2O2)固体更好,因而具有广泛的应用前景。某小组合成该固体双氧水的实验步骤和装置示意图如下:
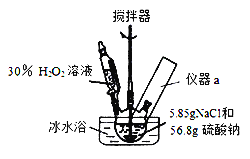
Ⅰ.合成:往三颈瓶中加入56.8g硫酸钠和5.85gNaCl的固体混合物,开启搅拌器;将稍过量的(约70mL)30%H2O2溶液在20~30min内逐滴分批加入。并控制反应温度15~35℃,加完料后持续搅拌15min,反应结束后过滤,低温干燥得到产品。
Ⅱ.产品稳定性取Ⅰ中所得产品置于干燥器内保存一个月,并分别在放置前、放置后取一定质量的样品溶于水,加适量稀硫酸酸化,用0.1000mol/L酸性高锰酸钾滴定,测定产品中双氧水的含量,以此分析产品的稳定性.所得实验数据如下表:
数据
时间
样品取用数量(g)
平均V(KMnO4)/mL
放置前测定
a
25.00
放置一个月后测定
a
24.90
已知:a.H2O2不稳定,加热,加入某些金属离子或加碱均有利于其分解
b.产品稳定性=
 ×100%
×100%请回答下列问题:
(1)装置图里方框中应添加仪器a,其名称为_______________________;写出合成4Na2SO4•2H2O2•NaCl的化学方程式:_____________________________。
(2)该合成反应过程中,关键是控制温度,其合理的措施是:______________。
A.逐滴滴加H2O2 B.选用Na2SO4和NaCl固体,而不用其饱和溶液
C.不断搅拌 D.冰水浴
(3)该合成反应过程中30%的H2O2溶液不应大大过量的原因________________。
(4)4Na2SO4•2H2O2•NaCl固体比过碳酸钠(2Na2CO3•3H2O2)固体更稳定的可能原因是__________。
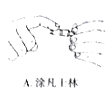
(5)产品分析实验时,高锰酸钾溶液装于滴定管中,当滴定到达终点时的现象是_________________。下列关于该滴定实验过程中的仪器选择和操作都正确的是_____________
A.
 B.
B.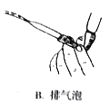 C.
C. D.
D.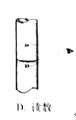
(6)该产品的“产品稳定性”=___________________。
高三化学实验题中等难度题查看答案及解析