-
能源问题是人类生存和社会发展的重要问题,下列关于能源问题的说法正确的是( )
A. 氢气是具有热值高、无污染等优点的燃料
B. 采用新技术开采煤、石油和天然气,以满足经济发展的需要
C. 煤燃烧是化学能只转化为热能的过程
D. 风能是太阳能的一种转换形式,所以风能属于二次能源
高三化学单选题简单题查看答案及解析
-
合理利用燃料减小污染符合“绿色奥运”理念,下列关于燃料的说法正确的是( )
A.“可燃冰”是将水变为油的新型燃料
B.氢气是具有热值高、无污染等优点的燃料
C.乙醇是比汽油更环保、不可再生的燃料
D.石油和煤是工厂经常使用的可再生的化石燃料
高三化学单选题简单题查看答案及解析
-
下列说法正确的是( )
A.“可燃冰”是将水变为油的新型燃料,具有热值高、无污染等优点
B.淀粉、纤维素和油脂都是天然高分子化合物
C.N2(g)+3H2(g)
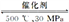 2NH3(g)采用高温、高压的条件有利于提高氨的产量
2NH3(g)采用高温、高压的条件有利于提高氨的产量D.催化剂能够加快化学反应速率是由于其参与了化学反应并改变了反应的路径,使反应所需的活化能降低
高三化学单选题中等难度题查看答案及解析
-
化学与生活、生产、环境密切相关,下列有关说法错误的是
A. K2FeO4和明矾都可做水处理剂,但工作原理不完全相同
B. 氢能是一种新型能源,具有热值高、资源丰富、无毒、无污染的优点
C. 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀
D. 合成氨工业中,使用催化剂不能提高H2和N2的转化率
高三化学选择题简单题查看答案及解析
-
全氮类物质具有高密度、超高能量及爆轰产物无污染等优点。中国科学家成功合成全氮阴离子N5-,N5-是制备全氮类物质N5+N5-的重要中间体。下列说法中,不正确的是
A. 全氮类物质属于绿色能源 B. 每个N5+中含有35个质子
C. N5+N5-属于离子化合物 D. N5+N5-结构中含共价键和离子键
高三化学单选题简单题查看答案及解析
-
全氮类物质具有高密度、超高能量及爆轰产物无污染等优点。中国科学家成功合成全氮阴离子N5-,N5-是制备全氮类物质N5+N5-的重要的中间体。下列说法中,不正确的是( )
A. 全氮类物质属于绿色能源 B. 每个N5+中含有35个质子
C. N5+N5-结构中只有共价键 D. N5+N5-爆炸时,它既是氧化剂又是还原剂
高三化学单选题中等难度题查看答案及解析
-
[2016·天津]氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是 (至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式: 。
(2)氢气可用于制备H2O2。已知:
H2(g)+A(l)
B(l) ΔH1
O2(g)+B(l)
A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+O2(g)
H2O2(l)的ΔH 0(填“>”、“<”或“=”)。
(3)在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)
MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是 。
a.容器内气体压强保持不变
b.吸收y mol H2只需1 mol MHx
c.若降温,该反应的平衡常数增大
d.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为 。
(5)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4。同时获得氢气:Fe+2H2O+2OH−
+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
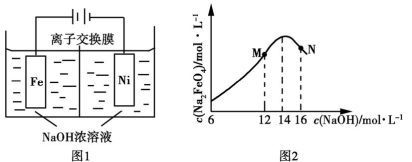
①电解一段时间后,c(OH−)降低的区域在 (填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因为 。
③c(Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因: 。
高三化学填空题中等难度题查看答案及解析
-
硼氢化物NaBH4(B元素的化合价为+3价)燃料电池(DBFC),由于具有比能量高、产物清洁无污染和燃料易于储存和运输等优点,被认为是一种很有发展潜力的燃料电池,其工作原理如图所示,下列说法正确的是
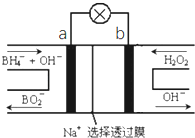
A.放电时,每转移2mol电子,理论上需要消耗9.5gNaBH4
B.电极a采用MnO2,MnO2既作电极材料又有催化作用
C.电池放电时Na+从b极区移向a极区
D.电池的负极反应为
+2H2O﹣8e-=
+8H+
高三化学单选题中等难度题查看答案及解析
-
氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是_________(至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:____________。
(2)氢气可用于制备H2O2。已知:
H2(g)+A(l)=B(l) ΔH1
O2(g)+B(l)=A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+ O2(g)= H2O2(l)的ΔH____0(填“>”、“<”或“=”)。
(3)在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)
MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
a.容器内气体压强保持不变
b.吸收y mol H2只需1 mol MHx
c.若降温,该反应的平衡常数增大
d.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______。
(5)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH−
FeO42−+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
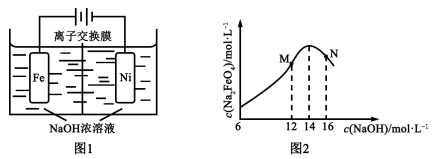
①电解一段时间后,c(OH−)降低的区域在_______(填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______。
③c( Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:_____________。
高三化学填空题困难题查看答案及解析
-
氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是_________(至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:____________。
(2)氢气可用于制备H2O2。已知:
H2(g)+A(l)=B(l) ΔH1
O2(g)+B(l)=A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+ O2(g)= H2O2(l)的ΔH____0(填“>”、“<”或“=”)。
(3)在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)
MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
a.容器内气体压强保持不变
b.吸收y mol H2只需1 mol MHx
c.若降温,该反应的平衡常数增大
d.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______。
(5)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH−
FeO42−+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
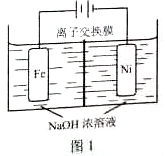
①电解一段时间后,c(OH−)降低的区域在_______(填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______。
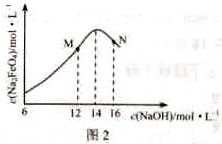
③c( Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c( Na2FeO4)低于最高值的原因:_____________。
高三化学简答题极难题查看答案及解析