-
已知:H+(aq)+OH-(aq)= H2O(l) ΔH=-57.3 kJ/ mol,计算下列中和反应中放出的热量:
(1)用20 g NaOH配成的稀溶液跟足量的稀盐酸反应,能放出________kJ的热量。
(2)用0.1 mol Ba(OH)2配成的稀溶液跟足量的稀硝酸反应,能放出________kJ的热量。
(3)用1 mol醋酸稀溶液和足量NaOH稀溶液反应,放出的热量________(填“大于”、“小于”或“等于”)57.3 kJ,理由是 。
(4)1 L 0.1 mol/L NaOH溶液分别与①醋酸溶液、②浓硫酸、③稀硝酸恰好反应时,放出的热量分别为Q1、Q2、Q3(单位:kJ)。则它们由大至小的顺序为________。
高一化学填空题中等难度题查看答案及解析
-
(10分)已知H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol,计算下列中和反应中放出的热量。
(1)用20 gNaOH配成稀溶液跟足量稀盐酸反应,放出 ____________ 热量。
(2)用0.1mol Ba(OH)2配成稀溶液跟足量稀硝酸反应放出 ____________热量。
(3)用1mol醋酸稀溶液和足量NaOH溶液反应,放出的热量____________(大于、小于、等于)57.3kJ,理由是_______________________
(4)实验测得苯(l)的标准燃烧热为3265kJ/mol,写出苯(l)燃烧时燃烧热的热化学方程式_________________
高一化学填空题中等难度题查看答案及解析
-
已知稀溶液中H+(aq)+OH-(aq)===H2O(l),生成1 mol H2O(l)放出57.3 kJ 热量。下列过程中放出热量为57.3 kJ的是
A. 1 mol H2SO4与足量的NaOH溶液反应
B. 稀盐酸与氨水反应生成1 mol H2O(l)
C. 稀盐酸与稀Ba(OH)2溶液反应生成1 mol H2O(l)
D. 稀NaOH与98%浓硫酸反应生成 1 mol H2O(l)
高一化学单选题简单题查看答案及解析
-
已知H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1。回答有关中和反应的问题:
(1)用0.1 mol NaOH配成稀溶液与足量稀硝酸反应,能放出________热量。
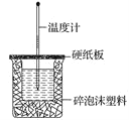
(2)如图装置中缺少的仪器名称是_____,碎泡沫塑料的作用______。
(3)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会___________(填“偏大”、“偏小”或“无影响”)。
高一化学实验题简单题查看答案及解析
-
已知H+(aq)+OH—(aq)=H2O(l)放出的57.3KJ,下列反应中放出57.3KJ热量的有 ( )
①KHSO4(aq)+KOH(aq)= K2SO4(aq)+ H2O(l) ②H2SO4(aq)+Ba(OH)2=BaSO4↓+2 H2O(l)
③HCl(aq)+ NaOH(aq)=NaCl (aq)+ H2O(l) ④HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+ H2O(l)
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2 H2O(l) ⑥CH3COOH(aq)+NaOH(aq)= CH3COONa(aq)+ H2O(l)
A①③ B.③④ C.④⑤ D.②⑥
高一化学选择题中等难度题查看答案及解析
-
已知H+(aq)+OH—(aq)=H2O(l)放出的57.3KJ,下列反应中放出57.3KJ热量的有 ( )
①KHSO4(aq)+KOH(aq)= K2SO4(aq)+ H2O(l) ②H2SO4(aq)+Ba(OH)2=BaSO4↓+2 H2O(l)
③HCl(aq)+ NaOH(aq)=NaCl(aq)+ H2O(l) ④HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+ H2O(l)
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2 H2O(l) ⑥CH3COOH(aq)+NaOH(aq)= CH3COONa(aq)+ H2O(l)
A.①③ B.③④ C.④⑤ D.②⑥
高一化学选择题中等难度题查看答案及解析
-
已知H+ +OH- = H2O生成1 mol H2O放出热量57.3 kJ,下列反应中放出57.3 kJ热量的是
A.1 mol稀H2SO4与足量NaOH溶液反应
B.稀盐酸与氨水反应生成1 mol H2O
C.稀盐酸与稀Ba(OH)2溶液反应生成1 mol水
D.稀NaOH与98.3%硫酸生成1 mol水
高一化学选择题中等难度题查看答案及解析
-
已知H+ +OH- = H2O生成1 mol H2O放出热量57.3 kJ,下列反应中放出57.3 kJ热量的是( )
A.1 mol稀H2SO4与足量NaOH溶液反应 B.稀盐酸与氨水反应生成1 mol H2O
C.稀盐酸与稀Ba(OH)2溶液反应生成1 mol水 D.稀NaOH与98.3%硫酸生成1 mol水
高一化学选择题简单题查看答案及解析
-
已知H+ +OH- ====H2O生成1 mol H2O放出热量57.3 kJ,下列反应中放出57.3 kJ热量的是( )
A.1 mol稀H2SO4与足量NaOH溶液反应
B.稀盐酸与氨水反应生成1 mol H2O
C.稀盐酸与稀Ba(OH)2溶液反应生成1 mol水
D.稀NaOH与95%浓硫酸反应生成1 mol水
高一化学选择题简单题查看答案及解析
-
已知H++OH-=H2O,该反应每生成1mol H2O (l)放出57.3kJ的热量。下列反应过程中放出热量为57.3kJ的是(提示:弱电解质的电离是吸热过程)( )
A. 含1mol H2SO4的稀硫酸与足量的NaOH溶液反应
B. 稀盐酸与氨水反应生成1mol H2O (l)
C. 稀盐酸与Ba(OH)2溶液反应生成1mol H2O (l)
D. NaOH稀溶液与98%的浓硫酸反应生成1mol H2O (l)
高一化学单选题中等难度题查看答案及解析