-
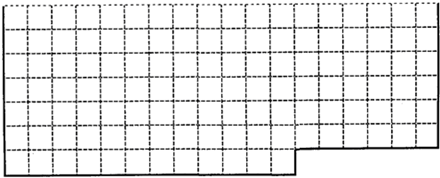
(1)下表中的实线是元素周期表部分边界,请在表中用实线画出金属元素的边界(实线内的元素全是金属元素)
(2)元素甲是第三周期原子半径最小的主族元素,化合物A是由甲元素等非金属元素组成的离子化合物写出其化学式________,
(3)元素乙是第三周期原子半径最小的金属元素,丙是短周期元素中原子半径最大的元素,用电子式表示丙在甲单质中加热反应生成B的形成过程________.
丙在空气中加热反应生成的物质中含有的化学键是________.
写出乙、丙两种元素的最高价氧化物的水化物相互反应的离子方程式:________.
(4)丁元素与丙元素同族并位于其下一周期,写出它与冷水反应的化学方程式:________.
-
(1)表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界________。

(2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)
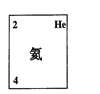
写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
____
(3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:________>________(用元素符号表示),甲、乙的最高价氧化物水化物相互反应的离子方程式为:________
(4)元素周期表体现了元素周期律,即元素的性质随着_________的递增呈现____的变化。
-
(1)上表中的实线是元素周期表部分边界,请在表中用实线画出金属元素的边界(实线内的元素全是金属元素)
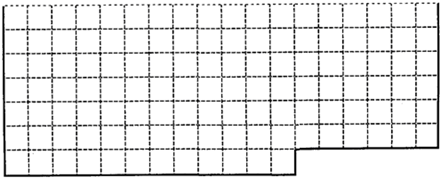
(2)元素甲是第三周期ⅦA族元素,化合物A是由甲元素等非金属元素组成的离子化合物写出其化学式________,
(3)元素乙是第三周期原子半径最小的金属元素,丙是短周期元素中原子半径最大的元素,用电子式表示丙在空气中加热反应生成B的形成过程________.B中含有的化学键是________
(4)化合物C是由甲元素和乙元素形成的化合物,将化合物A与化合物C等物质的量溶于水中,向其中滴加过量的2mol•L-1氢氧化钠溶液,直至形成透明溶液.请根据实验现象出现的先后顺序,依次写出离子方程式:________________________.
(5)实验中丙元素的鉴别方法________(不写过程)与现象________.
-
下表是元素周期表的一部分.表中所列的字母分别代表某一化学元素.
(1)下表中的实线是元素周期表部分边界,请用铅笔在表中用实线补全元素周期表边界.
(2)写出相应字母所代替的元素(填写元素符号)
b________ e________ g________ i________
(3)利用上表a-i九种元素完成下列填空:(请用具体化学式完成,否则不给分)
①这些元素中最活泼的金属元素是________,最活泼的非金属单质是________.
②这些元素中所能形成的气态氢化物溶于水得到的溶液,酸性最强的是________,溶液呈碱性的是________.用两根玻璃棒分别蘸取上述两种浓溶液在空中相遇,可观察到的现象为________.
③写出h的最高价氧化物对应的水化物与f的最高价氧化物对应的水化物发生反应的离子方程式________.
④写出h在空气中燃烧的产物的电子式________,该产物化学键的类型为________、________.
-
(普高完成)下表中的实线表示元素周期表的部分边界.①-⑥分别表示元素周期表中对应位置的元素.
(1)请在表中用粗实线补全元素周期表边界.
(2)上述元素中非金属性最强的元素是______,(填元素名称)⑦的原子序数为______.
(3)写出由④的氢化物与⑧的氢化物反应所组成的化合物的电子式______,上述元素中的某一元素的最高价氧化物对应的水化物是强碱其水溶液能和元素⑥的单质发生反应,其反应方程式为______.
-
(10分)下表中的实线表示元素周期表的部分边界。①-⑥分别表示元素周期表中对应位置的元素。

(1)请在表中用粗实线补全元素周期表边界。
(2)②号元素位于第周期________族。
(3)写出由①、③两种元素组成的摩尔质量最小的化合物的电子式________,上述元素中能和⑤号元素形成的原子晶体的化学式是________
(4)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的化学反应方程式为_____________,该生成物质含有的化学键类型是________。
-
下表中的实线表示元素周期表的部分边界,a-1分别表示周期表中对应位置的元素。

(1)请在上表中用实线补全元素周期表边界____。
(2)表中所列元素,不属于短周期元素有____,不属于主族元素的有___(填相应的元素符号)
(3)指出下列元素在周期表中的位置:
①b元素位于第___周期___族;
②g元素位于第___周期___族;
③i元素位于第___周期___族;
(4)①写出b与c的化合物(温室气体)电子式:___________;
②用电子式表示k与h化合物形成过程:__________。
-
(17分)
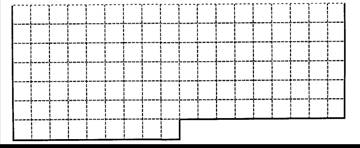
Ⅰ.上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界,并画出金属和非金属的分界线,用阴影画出铁元素所在的族。
Ⅱ. A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是________,画出B元素简单离子结构示意图________,乙物质的电子式是________
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)________
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是________
(4)简述比较D与E金属性强弱的实验方法:________
(5)E的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用)其反应方程式为________
-
下表中的实线表示元素周期表的部分边界.①~⑤分别表示元素周期表中对应位置的元素.
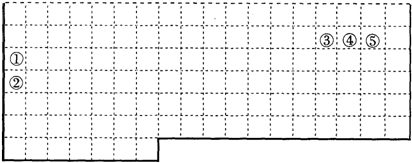
(1)请在上表中用实线补全元素周期表边界.
(2)元素③氢化物的化学式为______.
(3)元素④-般在化合物中显______价,但与______形成化合物时,所显示的价态则恰好相反.
-
Ⅰ.上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界,并画出金属和非金属的分界线,用阴影画出铁元素所在的族.
Ⅱ.A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期.C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙.A原子的最外层电子数比次外层电子层多3个.E是地壳中含量最高的金属元素.根据以上信息回答下列问题:
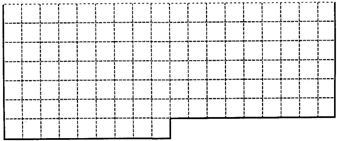
(1)D元素在周期表中的位置是________,画出B元素简单离子结构示意图________,乙物质的电子式是________
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)________
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是________
(4)简述比较D与E金属性强弱的实验方法:________
(5)E的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用)其反应方程式为________.








