-
下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)
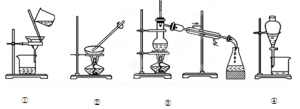
从海水中提取水:从KCl溶液中获取KCl晶体
分离CaCO3和水;分离植物油和水
-
(1)下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)
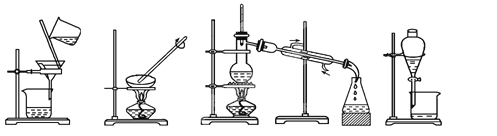
① ② ③ ④
从海水中提取水:____________;从KCl溶液中获取KCl晶体:____________;
分离CaCO3和水:____________;分离植物油和水:____________。
(2)现有甲、乙两瓶无色溶液,已知它们可能为AlCl3溶液和NaOH溶液。现分别将一定体积的甲、乙两溶液混合,具体情况如下表所示,请回答:
| 实验① | 实验② | 实验③ |
| 取甲瓶溶液的量 | 400 mL | 120 mL | 120 mL |
| 取乙瓶溶液的量 | 120 mL | 440 mL | 400 mL |
| 生成沉淀的量 | 1.56 g | 1.56 g | 3.12 g |
①甲瓶溶液为________溶液。
②乙瓶溶液为________溶液,其物质的量浓度为________mol·L-1。
【答案】 ③ ② ① ④ AlCl3 NaOH 0.5
【解析】(1)水易挥发,海水中提取水可用蒸馏的方法,答案选③;从 KCl溶液中获取KCl晶体,可用蒸发的方法,答案选②;CaCO3不溶于水,分离CaCO3和水,可用过滤的方法,答案选①;植物油和水互不相溶,分离植物油和水,可用分液的方法,答案选④;
(2)氯化铝滴入NaOH溶液中,开始氢氧化钠过量,发生反应AlCl3+4NaOH═NaAlO2+3NaCl+2H2O,然后发生反应:3NaAlO2+AlCl3+6H2O=4Al(OH)3↓+3NaCl;氢氧化钠溶液滴入AlCl3溶液中,开始发生反应:AlCl3+3NaOH═Al(OH)3↓+3NaCl,然后发生反应:Al(OH)3+NaOH═NaAlO2+2H2O,由②和③可知,一定量的甲与乙反应时,乙的量越多,生成的沉淀越少,则乙为NaOH溶液,即甲为AlCl3溶液,乙为NaOH溶液,由实验①②可知,实验①中NaOH不足,AlCl3有剩余,根据AlCl3+3NaOH═Al(OH)3↓+3NaCl,1.56g沉淀的物质的量为 =0.02mol,则NaOH的物质的量为0.02mol×3=0.06mol,故NaOH溶液的物质的量浓度为0.06mol/0.12L=0.5mol/L。
=0.02mol,则NaOH的物质的量为0.02mol×3=0.06mol,故NaOH溶液的物质的量浓度为0.06mol/0.12L=0.5mol/L。
【题型】综合题
【结束】
18
(1)向AlCl3溶液中,滴加少量NaOH溶液,现象是________________________
继续滴加NaOH溶液至过量,现象是_______________。
(2)钠与水反应的离子方程式为_______________,该反应中氧化剂是_______________,产生1mol H2时,转移电子的物质的量为_______________mol。
(3)经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O
①该反应的氧化剂是_______,被氧化的是_________元素。
②若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为___________。
-
观察下列实验装置图,按要求作答:
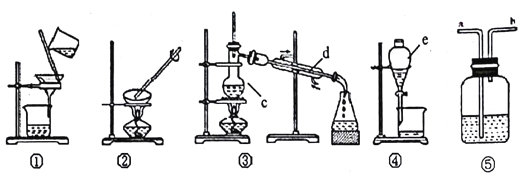
(1)装置中c、d、e 的名称分别为_________
(2)分离下列物质,需要在哪套装置中进行?
I.干燥H2,可采用______(填装置序号) 装置
II.除去食盐溶液中的水,可采用_____ (填装置序号)装置
III. 淡化食盐水,可采用___ (填装貿序号) 装置
IV.实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可采用____ (填装置序号) 装置除去Ca(OH)2溶液中悬浮的CaCO3微粒
V.分离碘水中的碘应先选择装置_____(填装置序号), 进行______和____操作,再用装置____(填装置序号) 进行______操作。
-
(18分)下图为两套实验装置。
(1)写出下列仪器的名称:
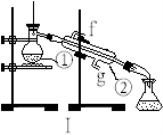
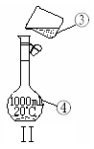
① ;② 。
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填序号)
(3)若利用装置I制取蒸馏水,还缺少的仪器是 ,将仪器补充完整后进行实验,冷却水从 口进。
(4)现需配制1.0 mol·L-1的NaOH溶液240mL,其中装置II是某同学配制此溶液时转移操作的示意图,图中有两处错误分别是 、 。
(5)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为_____________________。
(6)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为_________g,该同学应称量_________g NaOH。
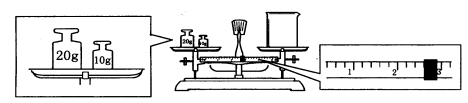
(7)在配制过程中,如果其他操作都是正确的,下列操作会引起浓度偏高的是__________。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量溶液洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
-
下图为两套实验装置。
(1)写出下列仪器的名称:
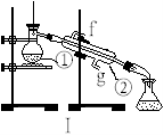
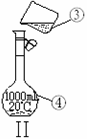
① ;② 。
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填序号)
(3)若利用装置I制取蒸馏水,还缺少的仪器是 ,将仪器补充完整后进行实验,冷却水从 口进。
(4)现需配制1.0 mol·L-1的NaOH溶液240mL,其中装置II是某同学配制此溶液时转移操作的示意图,图中有两处错误分别是 、 。
(5)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为_____________________。
(6)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为______g,该同学应称量______g NaOH。
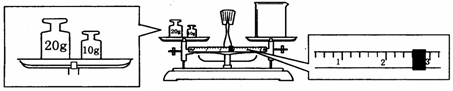
(7)在配制过程中,如果其他操作都是正确的,下列操作会引起浓度偏高的是__________。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量溶液洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
-
下图为两套实验装置。
(1)写出下列仪器的名称:
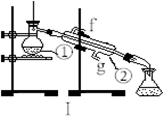
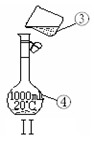
① ;② 。
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填序号)
(3)若利用装置I制取蒸馏水,还缺少的仪器是 ,将仪器补充完整后进行的实验操作的名称为: ,冷却水从 口进。
(4)某学生欲用11.9 mol/L浓盐酸和蒸馏水配制480mL物质的量浓度为0.400 mol/L的稀盐酸.
①其中装置II是某同学配制此溶液时转移操作的示意图,图中有两处错误分别是 、 。
②将下列操作填写完整,并排列其正确的操作顺序(字母表示,每个字母只用一次) _ _ _ _;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取浓盐酸 _________ mL,注入烧杯中,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其混合均匀
C.将已冷却的盐酸沿玻璃杯注入 _________ 中
D.将容量瓶盖紧,颠倒摇匀
E.改用 _________ 加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度线 _________ 处.
③若配制时,因加水不慎略超过了容量瓶刻度线,此时实验应如何继续进行?________
④在配制过程中,如果其他操作都是正确的,下列操作会引起浓度偏高的是__________。
a没有洗涤烧杯和玻璃棒
b转移溶液时不慎有少量溶液洒到容量瓶外面
c容量瓶不干燥,含有少量蒸馏水
d定容时俯视刻度线
e定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
-
实验室需要0.5 mol·L-1硫酸溶液480 ml。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液需要的是______(填序号),在使用如下B、C两种仪器前都应进行的操作 。

(2)下列操作中,容量瓶所不具备的功能有______ __(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
(3)根据计算,用量筒量取18.4 mol·L-1的浓硫酸体积为___ ___ ml, 如果实验室有10 mL、15 mL、20 mL量筒,选用 ml的量筒最好。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.5 mol·L-1(填“大于”、“等于”或“小于”,下同)。若浓硫酸在烧杯中溶解后,未冷却至室温就转移至容量瓶,则所得溶液浓度________0.5 mol·L-1。
-
观察下列实验装置图,试回答下列问题:
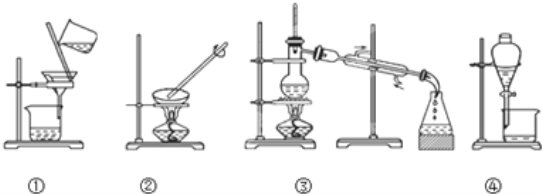
⑴写出图中实验操作对应的名称 ①:_______________ 、 ③:______________ 。
⑵下列实验需要在哪套装置中进行(填序号): a、分离植物油和水: ____________ ; b、从海水中提取蒸馏水: __________ ;
⑶装置①中玻璃棒的作用是__________________________________;
⑷ 实验室需要490mL 0.5mol•L-1 NaOH溶液,请回答下列问题:
①需称取 ___________g的烧碱固体.
②配制的玻璃仪器除烧杯和玻璃棒、胶头滴管,还需要___________________________。
③下列各项中,可能导致实际浓度偏高的是 _________(填标号).
A.定容时,仰视容量瓶的刻度线
B.NaOH溶解时放出大量的热,未冷却立即配制溶液
C.溶解NaOH固体之后的烧杯未洗涤
D.向容量瓶中转移溶液时不慎洒出
-
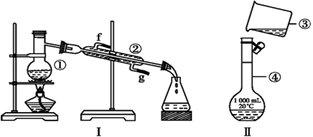
(1)写出下列仪器的名称:
① ,② ,④ 。
(2)仪器①~④中,使用时必须检查是否漏水的是 (填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器是 ,将仪器补充完整后进行的实验操作的名称为 ;②的进水口是 (填“f”或“g”)。
-

(1)写出下列仪器的名称:a. b.
(2)仪器a~e中,使用前必须检查是否漏水的有 。(填序号)
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 。将仪器补充完整后进行实验,加热一会儿发现未加沸石或碎瓷片,应该选择哪种处理方式 。
A.冷却再加 B趁热加 C不采取任何方式
(4)现需配制0.1mol/·LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是 。(写一条)除了图中给出的仪器和托盘天平外,为完成实验还需要的玻璃仪器有: 、 ;
②根据计算得知,所需NaOH的质量为___ ___g。
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) 。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
④配制0.1 mol· L-1NaOH溶液的实验中,如果出现以下操作:
A.称量时用了生锈的砝码
B.容量瓶未干燥即用来配制溶液
C.往容量瓶转移时,有少量液体溅出
D.未洗涤溶解NaOH的烧杯
E.定容时俯视刻度线
上述操作中所配溶液的物质的量浓度偏大的有(填写字母)__________

=0.02mol,则NaOH的物质的量为0.02mol×3=0.06mol,故NaOH溶液的物质的量浓度为0.06mol/0.12L=0.5mol/L。













