-
NOx在阳光的作用下会引起光化学烟雾,从而造成严重的大气污染。火力发电厂烟气中含有大量氮氧化物,必须对燃烧后的烟气进行处理,其原理如下(已知:燃烧系统排放烟气中的NOx,90%以上是NO):

请回答:
(1)NO2气体的颜色为______。
(2)下列物质可作试剂A的是______(填字母)。
a.O3 b.CO c.NH3 d.ClO2
(3)试剂B可使用Na2SO3溶液,该反应的化学方程式为______。
(4)NO2还可以用NaOH溶液吸收(原理:2NO2+2NaOH===NaNO2+NaNO3+H2O)。取一定量 NO2用过量的V1 mL c1 mol·L−1NaOH溶液吸收完全,剩余NaOH用V2 mL c2 mol·L−1 H2SO4溶液恰好中和,则被吸收的NO2物质的量是______。
-
工业燃烧煤、;石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对 废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ脱硝:
己知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) △H=+l33kJ·mol-1
H2O(g)=H2O(l) △H=-44kJ·mol-1
在催化剂存在下,H2还原NO2可生成水蒸气和其它无毒物质的热化学方程式为:____________。
Ⅱ.脱碳:在2L的密闭容器中充入2mo1 CO2和6mol H2,在适当的催化剂作用下发生反应:
CO2(g)+3H2(g) CH3OH(l)+H2O(l) △H<0
CH3OH(l)+H2O(l) △H<0
①该反应自发进行的条件是___________(填“”低温或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是________(填字母)
a.混合气体的平均摩尔质量保持不变
b. CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d. 混合气体的密度保持不变
e. 1mol CO2生成的同时有3 mul H―H键断裂
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,请画出t2~t4CO2浓度随时间的变化。______

(2)改变温度,使反应CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) △H<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| 反应I:恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| l0min | | 4.5 | | |
| 20min | 1 | | | |
| 30min | | | 1 | |
| 反应Ⅱ:绝热恒容 | 0min | 0 | 0 | 2 | 2 |
① 达到平衡时,反应I、Ⅱ对比:平衡常数K(I)_____K(Ⅱ)(填“>”“<”或“=”下同);平衡时CH3OH的浓度 c(I)______c(Ⅱ)。
②对反应I,前10min内的平均反应速率v(CH3OH)=_________。在其他条件不变的情况下,若30min时只改变温度T2℃,此时H2的物质的量为3.2mol,则T1________T2(填“>”“<”或“=”)。
-
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境问题。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g) + 4NO2(g) =4NO(g) + CO2(g) + 2H2O(g) △H1=-574 kJ·mol-1
CH4(g) + 4NO(g) =2N2(g) + CO2(g) + 2H2O(g) △H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为 。
(2)脱碳。将CO2转化为甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
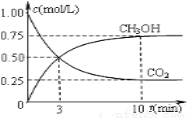
在体积为1L的固定容积的密闭容器中充入1 mol CO2和3 mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如右图所示。试回答:
①0—10 min内,氢气的平均反应速率为___________mol/(L·min)。
②下列选项能说明该反应已达到平衡状态的是 。
A.v(H2)=3v(CO2)
B.容器内气体密度不变
C.单位时间内,形成2molC=O,同时断裂3molH—H
D.容器内温度不变
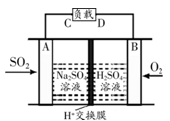
(3)脱硫。有学者想利用如下图所示装置用原电池原理将SO2转化为重要的化工原料,A、B是惰性电极。则电子流出的电极为____(用A或B表示),A极的电极反应式为_ ___。
-
研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义。
(1)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) △H=-a KJ·mol-1 (a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-b KJ·mol-1 (b>0)
若用标准状况下3.36LNO2氧化CO至CO2(NO2完全反应)的整个过程中转移电子的物质的量为_____mol,放出的热量为_________ kJ(用含有a和b的代数式表示)。
(2)己知下列反应的反应热:
①CH3COOH(1)+2O2(g)=2CO2(g)+2H2O(1) △H=-870.3kJ/mo1
②C(s)+O2(g) =CO2(g) ΔH=-393.5kJ/mo1
③2C(s)+2H2(g)+O2(g) =CH3COOH(1) ΔH=-488.3kJ/mo1
请写出H2燃烧热的热化学方程式______________________________________。
(3)在101kPa下,CH4(g)、H2(g)、C(s) 的燃烧热分别为890.3kJ/mol、285.8kJ/mol 和393.5kJ/mol,则CH4(g)分解为H2(g)、C(s)的热化学方程式_______________________________。
-
(9分)研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义。
(1)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
① CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1 (a>0)
② 2CO(g)+2NO (g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1 (b>0)
若用标准状况下 3.36LCO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为 mol,放出的热量为 kJ(用含有a和b的代数式表示)。
(2)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
②CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?
若1molCH4还原NO2至N2的整个过程中放出的热量为867kJ,则ΔH2=______________。
-
煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有的SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下(其它离子忽略不计):
| 离子 | Na+ | SO42− | NO3− | OH− | Cl− |
| c/(mol·L−1) | 5.5×10−3 | 8.5×10−4 | y | 2.0×10−4 | 3.4×10−3 |
(1)NaClO2属于钠盐,其中氯元素的化合价为_____;NaClO2的电离方程式为:____。
(2)SO2和NOx经NaClO2溶液吸收后转化为___________。此吸收过程中NaClO2所起的作用是__________。
(3)表中y=_______________。
-
我国北方大部分地区出现严重空气污染,其主要原因是化石燃料的大量使用。提高利用率,减少化石燃料燃烧所造成的环境污染,已成为人类面临的重大挑战。
(1)氢气是人类理想的能源。为了有效发展民用氢能源,首先必须制得廉价的氢气。下列可供开发且比较经济的制氢气的方法是________(填序号)。
①电解水 ②锌与稀硫酸反应 ③光解海水
制得氢气后还需要解决的问题是____(写出其中一个)。
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2+6H2O C6H12O6+6O2
C6H12O6+6O2
葡萄糖
b.CO2+3H2 CH3OH+H2O
CH3OH+H2O
c.CO2+CH4 CH3COOH
CH3COOH
d.2CO2+6H2 CH2===CH2+4H2O
CH2===CH2+4H2O
以上反应中,最节能的是________,原子利用率最高的是________。
(3)煤液化后可得到甲醇,甲醇在一定条件下与CO、H2作用生成有机物A,A发生加聚反应可生成高分子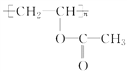 ,写出A的结构简式_________________。
,写出A的结构简式_________________。
-
下列有关大气污染说法中错误的是( )
A.SO2、NOx的大量排放会导致酸雨的发生
B.煤与石油的大量燃烧是造成SO2、NOx大量排放的主要因素
C.人类活动的气态污染物能全部进入大气中
D.烟尘、粉尘属于固体污染物
-
氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾。因此必须对含有氮氧化物的废气进行处理。
(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
 ====
====
在该反应中,氧化剂是________,还原剂是________ 。
(2)汽车尾气中含有一氧化氮和一氧化碳,经过排气管中的催化转化器转化为对大气无污染的物质。写出该反应的化学方程式:________。
(3)在一定条件下氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:________。
-
氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾.因此必须对含有氮氧化物的废气进行处理.
(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH═2NaNO2+H2O,在该反应中,氧化剂是______,还原剂是______.
(2)汽车尾气中含有一氧化氮和一氧化碳,经过排气管中的催化转化器转化为对大气无污染的物质.写出该反应的化学方程式:______ N2+2CO2




 ,写出A的结构简式_________________。
,写出A的结构简式_________________。