-
已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数, A的原子半径小于B,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图_______________。
(2)B、C、D三元素第一电离能由大到小的顺序为(用元素符号表示)______________。
(3)BD 中心原子杂化轨道的类型为______杂化;CA
中心原子杂化轨道的类型为______杂化;CA 的空间构型为_______(用文字描述)。
的空间构型为_______(用文字描述)。
(4)1 mol BC-中含有π键的数目为______。
(5)比较D、E元素最简单氢化物的稳定性_______(填化学式,用“>”连接),理由是_______________。
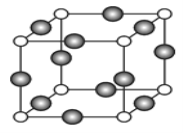
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是____,C原子的配位数是_____。若相邻C原子和F原子间的距离为anm,阿伏伽德罗常数为NA,则该晶体的密度为______g/cm3(用含a、NA的符号表示)。
-
短周期元素X、Y、Z、W原子序数依次增大,它们原子的最外层电子数之和为14.X与Z同主族.Y与W同主族,且X的原子半径小于Y.下列叙述正确的是( )
A.原子半径:Y<Z<W
B.Z在化合物中呈+1价
C.Y与W可形成离子化合物
D.Z的单质不能与X的氧化物反应
-
短周期元素X、Y、Z、W原子序数依次增大,它们原子的最外层电子数之和为14.X与Z同主族.Y与W同主族,且X的原子半径小于Y.下列叙述正确的是( )
A.原子半径:Y<Z<W
B.Z在化合物中呈+1价
C.Y与W可形成离子化合物
D.Z的单质不能与X的氧化物反应
-
X、Y、Z、W为短周期元素,且原子序数依次增大。X与W属于同一主族,X2-、Y+离子与氖原子具有相同的电子层结构,Z元素的周期序数等于主族序数。下列说法正确的是
A. 金属性:Z>Y
B. 原子半径:W>Z>Y>X
C. 元素X和Y只能形成一种化合物
D. Y、Z、W的最高价氧化物对应的水化物均能相互反应
-
X、Y、Z、W是短周期主族元素,且原子序数依次增大,X元素的周期序数等于其主族序数,且X为同主族元素中唯一非金属元素,Y元素的单质是一种强力漂白剂,Z元素形成的简单离子是同周期半径最小的离子,含元素W的一种化合物是木材防火剂的原料,下列叙述错误的是( )
A.上述四种元素的原子半径大小:Z>W>Y>X
B.Z的氢氧化物和NaHCO3均可中和过多的胃酸
C.X与Y只形成既含极性共价键又含非极性共价键的共价化合物
D.W与Y形成的化合物既是建筑材料,也是工艺品(玛瑙等)的原料
-
X、Y、Z、Q、W是原子序数依次增大的短周期主族元素,X的原子序数等于其电子层数,Y的原子最外层电子数是其电子层数的2倍,Z在同周期的主族元素中原子半径最大,元素Q的单质可被用作输电的导线,W单质在常温下呈气态。下列说法正确的是( )
A. 金属性:Q>Z
B. 原子半径:W>Q>Z
C. 化合物XW与ZW含有相同类型的化学键
D. 元素Z、Q的最高价氧化物对应的水化物能发生反应
-
短周期元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14。X与Z同主族,Y与W同主族,且X的原子半径小于Y。下列叙述正确的是
A.原子半径:Y<Z<W B.Z在化合物中呈+1价
C.Y与W可形成离子化合物 D.Z的单质不能与X的氧化物反应
-
短周期元素X、Y、Z、W原子序数依次增大,它们原子的最外层电子数之和为14。X与Z同主族.Y与W同主族,且X的原子半径小于Y。下列叙述不正确的是
A. 原子半径:Y<W <Z
B. Z在化合物中呈+1价
C. Y与W形成共价化合物
D. Z的单质不能与X的氧化物反应
-
短周期元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14。X与Z同主族,Y与W同主族,且X的原子半径小于Y。下列叙述正确的是
A.原子半径:Y<Z<W B. Z在化合物中呈+1价
C.Y与W可形成离子化合物 D.Z的单质不能与X的氧化物反应
-
W、M、X、Y、Z为原子序数依次增大的前四周期元素,非金属元素W所在周期数等于族序数;M最外层电子数是电子层数的两倍;X与M同族,X单质与O2反应生成化合物XO2;Y 是第三周期原子半径最小的元素;Z是生活中常见金属,既不属于主族,也不属于副族。回答下列问题:
(1) W与M可以形成多种化合物,写出其中最简单化合物的电子式_____________。
(2) 已知:①X的单质结构为(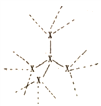 ,每个X原子周围都与4个X成键形成的庞大结构);化合物XO2结构为(
,每个X原子周围都与4个X成键形成的庞大结构);化合物XO2结构为(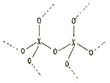 ,每个X与4个O成键,每个O都与2个X成键形成的庞大结构)。
,每个X与4个O成键,每个O都与2个X成键形成的庞大结构)。
②有关键能的数据如下表:
| 化学键 | X-O | O=O | X-X |
| 键能(kJ/mol) | 460 | 498.8 | 176 |
写出单质X 在O2中燃烧的热化学方程式________________________。(用具体元素符号书写方程式)
(3) 写出Z的单质与H2O反应的化学方程式_____________________________________。
(4)Y和Z形成的化合物的水溶液呈酸性的原因_______________________________(用离子方程式解释)。
中心原子杂化轨道的类型为______杂化;CA
的空间构型为_______(用文字描述)。

 ,每个X原子周围都与4个X成键形成的庞大结构);化合物XO2结构为(
,每个X原子周围都与4个X成键形成的庞大结构);化合物XO2结构为( ,每个X与4个O成键,每个O都与2个X成键形成的庞大结构)。
,每个X与4个O成键,每个O都与2个X成键形成的庞大结构)。