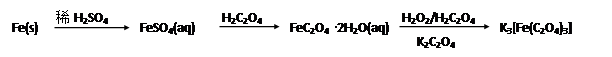-
草酸合铁酸钾晶体Kx[Fe(C2O4)y]·3H2O 是一种光敏材料,见光易分解,下面是一种制备草酸合铁酸钾晶体的实验流程。
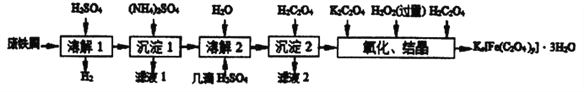
已知:(NH4)SO4、FeSO4·7H2O、莫尔盐[(NH4)2SO4·FeSO4·6H2O]的溶解度如表:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| (NH4)SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
| FeSO4·7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | — |
| (NH4)2SO4·FeSO4·6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(1)废铁屑在进行“溶解1”前,得用在5%Na2CO3溶液中加热数分钟,并洗涤干净.Na2CO3溶液的作用是___________________。
(2)“复分解”制备莫尔盐晶体的基本实验步骤是: 蒸发浓缩、_________、过滤、用乙醇洗涤、干燥。用乙醇洗涤的目的是_________ 。
(3)“沉淀2"时得到的FeC2O4·2H2O 沉淀需用水洗涤干净.检验沉淀是否洗涤干净的方法是_____。
(4)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是_________ 。
(5)为测定该晶体中铁的含量,某实验小组做了如下实验:
步骤1: 准确称量5.00g 草酸合铁酸钾晶体,配制成250mL 溶液
步骤2:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤3:用0.010mol/L KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO4-被还原成Mn2+.重复步骤2、步骤3 操作,滴定消耗 0.010mol/LKMnO4溶液19.98mL,实验测得该晶体中铁的质量分数为_____ (写出计算过程)。
-
K3[Fe(C2O4)3]·3H2O [三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂。实验室可用铁屑为原料制备,相关反应过程如下,请回下列问题:
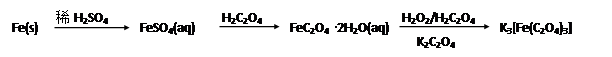
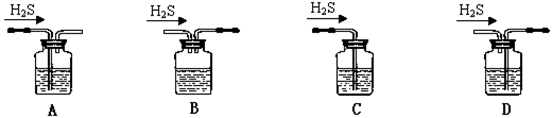
(1)铁屑中常含硫元素,因而在制备FeSO4时会产生有毒的H2S气体,该气体可用氢氧化钠溶液吸收。下列吸收装置正确的是________。
(2)在得到的FeSO4溶液中需加入少量的H2SO4酸化,目的是________,得到K3[Fe(C2O4)3]溶液后,加入乙醇的目的是________。
(3)晶体中所含结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤重复②~④至恒重,⑥计算。
步骤③需要在干燥器中进行的原因是________;
步骤⑤的目的是________。
(4) 可被酸性KMnO4溶液氧化放出CO2气体,所以实验产物中K3[Fe(C2O4)3]·3H2O含量测定可用KMnO4标准溶液滴定。
可被酸性KMnO4溶液氧化放出CO2气体,所以实验产物中K3[Fe(C2O4)3]·3H2O含量测定可用KMnO4标准溶液滴定。
①写出滴定过程中发生反应的离子方程式________;
②下列滴定操作中使滴定结果偏高的是________;
A.滴定管用蒸馏水洗涤后,立即装入标准液
B.锥形瓶在装待测液前未用待测液润洗
C.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
D.读取标准液体积时,滴定前仰视读数,滴定后俯视读数
③取产物10.0g配成100mL溶液,从中取出20mL于锥形瓶中,用浓度为0.1mol·L-1酸性KMnO4溶液滴定,达到滴定终点时酸性KMnO4溶液消耗24mL,计算产物中K3[Fe(C2O4)3]·3H2O的质量分数________。[已知摩尔质量M(K3[Fe(C2O4)3]·3H2O)=491g·mol-1]
-
三草酸合铁(III)酸钾K3[Fe(C204)3]·3H2O为绿色晶体,易溶于水,难溶于乙醇丙酮等有机溶剂。
I.三草酸合铁(III)酸钾晶体的制备
①将5g(NH4)2Fe(S04)2·6H2O晶体溶于20mL水中,加入5滴6mol/LH2SO4酸化,加热溶解,搅拌下加入25m饱和和H2C2O4溶液,加热,静置,待黄色的Fe C2O4沉淀完全沉降以后,倾去上层清液,倾析法洗涤沉定2--3次。
②向沉淀中加入10mL饱和草酸钾容液,水浴加热至40℃,用滴管缓慢滴加12mL5%H2O2,边加边搅拌并维持在40℃左右,溶液变成绿色并有棕色的沉淀生成。
③加热煮沸段时间后,再分两批共加入8mL饱和H2C2O4溶液(先加5mL,后慢慢滴加3mL)此时棕色沉淀溶解,变为绿色透明溶液。
④向滤液中缓慢加入10mL95%的乙醇,这时如果滤液浑浊可微热使其变清,放置暗处冷却,结晶完全后,抽滤,用少量洗条剂洗涤晶体两次抽干,干燥,称量,计算产率。
已知制各过程中涉及的主要反应方程式如下:
②6FeC2O4+3H2O2+6K2C2O4=4K3[Fe(C2O4)3]+2Fe(OH)3
步骤③2Fe(OH)3+3H2C2O4+3K2C2O4=2K3[Fe(C2O4)3]+6H2O
请回答下列各题:
(1)简达倾析法的适用范围____________。
(2)步骤③加热煮沸的目的是___________。
(3)步骤④中乙醇要缓慢加入的原因是_________。
(4)下列物质中最适合作为晶体洗涤剂的是_______(填编号)。
A.冷水 B.丙酮 C.95%的乙醇 D.无水乙醇
(5)如图装置,经过一系列操作完成晶体的抽滤和洗涤。请选择合适的编号,按正确的顺序补充完整(洗条操作只需要考虑一次):开抽气泵→a→____→b→d→c→关闭抽气泵。
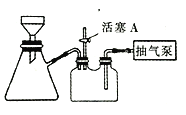
a.转移固体混合物 b.关活塞A c.开活塞A d.确认抽干 e.加洗涤剂洗涤
II.纯度的测定
称取1.000g产品,配制成250mL溶液,移取25.00mL溶液,酸化后用标定浓度为0.0100 mol/L 的高锰酸钾溶被滴定至终点,三次平行实验平均消耗高猛酸钾溶被24.00 mL。
(6)滴定涉及反应的离子方程式:____________。
(7)计算产品的纯度______(用质量百分数表示)。(K3[Fe(C204)3]·3H2O的相对分子质量为491)
-
三草酸合铁酸钾晶体[K3Fe(C2O4)3•xH2O]是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组实验步骤为:(1)称量9.820 g三草酸合铁酸钾晶体,配制成250 mL溶液。(2)取所配溶液25.00 mL于锥形瓶中,滴加酸性KMnO4溶液至C2O42-全部转化成CO2,同时MnO4-被转化成Mn2+,恰好消耗0. 1000 mol/L KMnO4溶液24.00 mL。[K3Fe(C2O4)3的相对分子质量为437] 下列说法正确的是
A.步骤(2)中KMnO4表现还原性
B.配制三草酸合铁酸钾溶液玻璃仪器只需烧杯和玻璃棒
C.样品中结晶水的物质的量为0.03 mol
D.该晶体的化学式为K3Fe(C2O4)3•3H2O
-
三草酸合铁酸钾晶体[K3Fe(C2O4)3•xH2O]是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组实验步骤为:
(1)称量9.820g三草酸合铁酸钾晶体,配制成250mL溶液.
(2)取所配溶液25.00mL于锥形瓶中,滴加酸性KMnO4溶液至C2O42-全部转化成CO2,同时MnO4-被转化成Mn2+,恰好消耗0.1000mol/LKMnO4溶液24.00mL.[K3Fe(C2O4)3的相对分子质量为437]
下列说法正确的是( )
A.步骤(2)中KMnO4表现还原性
B.配制三草酸合铁酸钾溶液玻璃仪器只需烧杯和玻璃棒
C.样品中结晶水的物质的量为0.03 mol
D.该晶体的化学式为K3Fe(C2O4)3•3H2O
-
(14分)三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·xH2O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量,某实验小组做了如下实验:
Ⅰ.称量4.910g三草酸合铁酸钾晶体,配制成250mL溶液。
Ⅱ.取所配溶液25.00mL于锥形瓶中,加稀硫酸酸化,滴加KMnO4溶液至草酸根(C2O42−)恰好全部氧化成二氧化碳,同时MnO4−被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液的黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
Ⅲ.用0.01000mol/L KMnO4溶液滴定步骤Ⅱ所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO4−被还原成Mn2+ 。
Ⅳ.重复步骤Ⅱ、步骤Ⅲ操作,滴定消耗0.01000mol/L KMnO4溶液19.98mL
请回答下列问题:
(1)滴定过程中需添加的指示剂是(若不需要请说明理由)
(2)加入锌粉的目的是 。
(3)写出步骤Ⅲ中发生反应的离子方程式 。
(4)实验测得该晶体中铁的质量分数为 ;X= 。
(5)在步骤Ⅱ中,若加入的KMnO4的溶液的量不够,则测得的铁含量 ;(选填“偏低”“偏高”“不变”,下同)若加入的锌粉的量不够,则测的铁的含量 。
-
三草酸合铁酸钾晶体{K3[Fe(C2O4)3]·xH2O}是一种光敏材料,为测定该晶体中铁的含量,某实验小组做了如下实验:
步骤一:称量4.00 g三草酸合铁酸钾晶体,配制成250 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO 被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010 mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02 mL,滴定中MnO 被还原成Mn2+。
被还原成Mn2+。
重复步骤二、步骤三操作,滴定消耗0.010 mol/L KMnO4溶液19.98 mL。
请回答下列问题:
(1)配制三草酸合铁酸钾溶液的操作步骤依次是:称量、________、转移、洗涤并转移、________、摇匀。
(2)加入锌粉的目的是________________ ___。
(3)写出步骤三中发生反应的离子方程式:________________________。
(4)实验测得该晶体中铁的质量分数为__________。在步骤二中,若加入的KMnO4溶液的量不够,则测得的铁含量________。(选填“偏低”、“偏高”或“不变”)
-
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·xH2O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量,某实验小组做了如下实验:
铁含量的测定
步骤一:称量5.00 g三草酸合铁酸钾晶体,配制成250 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时MnO4-被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤三:用0.010 mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02 mL,滴定中MnO4-被还原成Mn2+。重复步骤二、步骤三操作,滴定消耗0.010 mol/L KMnO4溶液分别为19.98 mL和20.00 mL。请回答下列问题:
(1)滴定过程中,高锰酸钾溶液应盛装在__________滴定管中(填“酸式”或“碱式”)。
(2)用离子方程式表示步骤二中涉及到的相关化学反应:________________; Zn + 2Fe3+ = 2Fe2+ + Zn2+。
(3)步骤三中滴定终点的判定:____________________。
(4)在步骤二中,若加入的KMnO4溶液的量不够,则测得的铁含量____________。在步骤三中,若滴定前仰视读数,滴定后俯视读数,则测得的铁含量__________。(选填“偏低”、“偏高”、“不变”)
(5)实验测得该晶体中铁的质量分数为__________。
-
三草酸合铁酸钾晶体(K3[Fe(C2O4) 3]·xH2O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
(1)铁含量的测定
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液。
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO4-被还原成Mn2+。
重复步骤二、步骤三操作,滴定消耗0.010mol/LKMnO4溶液19.98ml。
请回答下列问题:
①配制三草酸合铁酸钾溶液的操作步骤依次是:称量、 、转移、洗涤并转移、 摇匀。
②加入锌粉的目的是 。
③写出步骤三中发生反应的离子方程式 。
④实验测得该晶体中铁的质量分数为 。在步骤二中,若加入的KMnO4溶液的量不够,则测得的铁含量 。(选填“偏低”“偏高”“不变”)
(2)结晶水的测定
将坩埚洗净,烘干至恒重,记录质量;在坩锅中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至110℃,恒温一段时间,置于空气中冷却,称量并记录质量;计算结晶水含量。请纠正实验过程中的两处错误: ; 。
-
草酸合铁(Ⅲ)酸钾晶体[KxFe y(C2O4)z•nH2O]是一种光敏材料,为测定该晶体中各离子的含量和结晶水的含量,某实验小组实验步骤为:(1)称量9.820g草酸合铁酸钾晶体,加热脱水得无水物质量为8,74g.(2)将所得固体配制成250mL溶液.(3)取所配溶液25.00mL于锥形瓶中,滴加酸性KMnO4溶液发生反应:5C2O42﹣+2MnO4﹣+16H+=10CO2↑+2Mn2++8H2O,恰好消耗0.1000mol/L KMnO4溶液24.00mL.下列说法正确的是
A.9.820g晶体中含有C2O42﹣的物质的量为0.006mol
B.配制草酸合铁酸钾溶液玻璃仪器只需烧杯和玻璃棒
C.该晶体的化学式为K3Fe(C2O4)3•6H2O
D.9.820g样品中含K+的物质的量为0.06 mol