-
A、B、C、D、E 是原子序数依次增大的五种常
见元素,其中 A 是原子半径最小的元素,B 元素的一种核素可用于考古断代,D 元素的 s轨道和 p 轨道上的电子数相等且有2个未成对电子;E 是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满。请用元素符号或化学式回答下列问题:
(1)A、B、C、D 四种元素中,电负性最大的是________,第一电离能最大的是________。
(2)化合物 CA3 的沸点比化合物 BA4 的高,其主要原因是___________________________ 。
(3)A、B 形成的化合物与氢氰酸(HCN)反应可得丙烯腈(H2CCHCN),丙烯腈分子中的碳原子轨道杂化类型是__________。
(4)由 C 元素形成的一种离子与 BD2 互为等电子体,该离子的结构式为__________。
(5)基态 E 原子的核外电子排布式为:_____________________________;D、E 形成的某种化合物的晶胞结构示意图如下,该晶体的化学式为__________。

(6)向 E 的硫酸盐溶液中通入过量的 CA3,可生成[E(CA3)4]2+,1 mol [E(CA3)4]2+中含有σ 键的数目约为____________。
-
A、B、C、D、E是原子序数依次增大的五种常见元素,其中A是原子半径最小的元素,B元素的一种核素可用于考古断代,D元素的s轨道和p轨道上的电子数相等且有2个未成对电子;E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满。请用元素符号或化学式回答下列问题:
(1)A、B、C、D四种元素中,电负性最大的是___,第一电离能最大的是___。
(2)化合物CA3的沸点比化合物BA4的高,其主要原因是____。
(3)A、B形成的化合物M与氢氰酸(HCN)反应可得丙烯腈(H2C=CH—C≡N),则M的结构式为___,丙烯腈分子中碳原子轨道杂化类型是____。
(4)由C元素形成的一种离子与BD2互为等电子体,该离子的结构式为____。
(5)基态E原子的核外电子排布式为____,如图是D、E形成的某种化合物的晶胞结构示意图,该晶体的化学式为____。
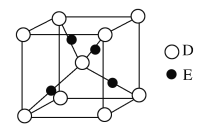
(6)向E的硫酸盐溶液中通入过量的CA3,可生成[E(CA3)4]2+,1mol[E(CA3)4]2+中含有σ键的数目约为___。
-
现有A、B、C、D、E五种短周期非金属元素,其原子序数依次增大。A是原子半径最小的元素,B元素的一种核素可用于考古断代,D元素的s轨道和p轨道上的电子数相等。C、E是同主族元素,它们的核外均有3个未成对电子。请回答下列问题:
(1)基态E原子有_____种能量不同的电子。
(2)六种元素中,电负性最大的是_______,第一电离能最大的是________(均填元素符号)。
(3)化合物CA3的沸点比化合物BA4的沸点高,其主要原因是____________。
(4)CD2-的立体构型是________,其中C原子的杂化类型为___________。
(5)C2A4溶于水电离方程式与CA3溶于水电离方程式相似,试写出C2A4在水溶液中的电离方程式____(写一步即可,要求用化学符号表示)。
(6)开发金属储氢材料是氢能的重要研究方向。MgA2是一种储氢材料,其晶胞结构如下图所示:
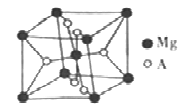
已知该晶胞的体积为Vcm3,则该晶胞的密度为_______g·cm-3(用V和NA表示)。
-
现有A、B、C、D、E五种短周期非金属元素,其原子序数依次增大。A是原子半径最小的元素,B元素的一种核素可用于考古断代,D元素的s轨道和p轨道上的电子数相等。C、E是同主族元素,它们的核外均有3个未成对电子。请回答下列问题:
(1)基态E原子有_____种能量不同的电子。
(2)六种元素中,电负性最大的是_______,第一电离能最大的是________(均填元素符号)。
(3)化合物CA3的沸点比化合物BA4的沸点高,其主要原因是____________。
(4)CD2-的立体构型是________,其中C原子的杂化类型为___________。
(5)C2A4溶于水电离方程式与CA3溶于水电离方程式相似,试写出C2A4在水溶液中的电离方程式____(写一步即可,要求用化学符号表示)。
(6)开发金属储氢材料是氢能的重要研究方向。MgA2是一种储氢材料,其晶胞结构如下图所示:
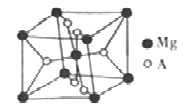
已知该晶胞的体积为Vcm3,则该晶胞的密度为_______g·cm-3(用V和NA表示)。
-
短周期主族元素X、Y、Z、Q、R、T的原子序数依次增大,X的原子半径是所有元素中最小的,Y元素是一种高效电池中的重要材料,Z的一种同位素可用于考古断代,R的最外层电子数是次外层电子数的3倍,T的单质可用于自来水消毒。下列说法错误的是( )
A.Y元素的单质在空气中燃烧只能生成一种氧化物
B.X、Q、R三种元素只能组成酸
C.简单离子半径:Q>R
D.简单氢化物稳定性:R>Q>Z
-
X、Y、Z、W、P是短周期主族元素,它们的原子序数依次增大,其中X的族序数=周期序数=原子序数,Y的最外层电子数等于其次外层电子数的2倍,它的一种核素常用于考古断代,W的一种单质被喻为“人类地球的保护伞”,P的最高正化合价与最低负化合价的代数和为4,下列说法正确的是( )
A.由X、Z、P三种元素形成的化合物只能是共价化合物
B.Y、Z、W、P氢化物的稳定性依次增强
C.食品中可适量添加PW2,起到去色、杀菌、抗氧化的作用
D.Y5X10W2能与碳酸氢钠反应的结构有三种
-
(14分)X、Y、Z、W、M是元素周期表中原子序数依次增大的五种元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | 元素周期表中核电荷数最小的元素 |
| Y | Y的一种核素常用于考古,其一种同素异形体为自然界最硬的物质 |
| Z | Z是大气中含量多的元素,其某些氧化物为大气中常见的污染物 |
| W | W是地壳中含量最高的金属元素 |
| M | 常见金属,单质呈紫红色 |
(1)W位于元素周期表第 周期第 族;W的简单离子半径比Z的简单离子半径 (填“大”或“小”)。
(2)Z原子的第一电离能比氧原子的 (填“大”或“小”);M的基态原子价电子排布式是
(3)X与Y可形成多种化合物,其中常用来切割或焊接金属的气体分子中σ键和π键之比是 ,空间构型是
(4)X与Z形成的最简单化合物用途非常广泛,试列举两种用途: 、 ;该化合物具有较强的还原性,加热时能将M的氧化物MO还原,写出该反应的化学方程式:____。
(5)可用YX4还原ZOx以消除其污染。已知:
YX4 (g) +4ZO2 (g)=4ZO(g)+YO2(g)+2X2O(g) △H= - 574 kJ·mol-1
YX4 (g)+4ZO(g)=2Z2 (g)十YO2 (g) +2X2O(g) △H = - 1160 kJ·mol-1
试写出用YX4还原ZO2至Z2的热化学方程式:____。
-
X、Y、Z、W、G是元素周期表中原子序数依次增大的五种元素。X元素是元素周期表中核电荷数最小的元素。Y的一种核素常用于考古,其一种同素异形体为自然界最硬的物质。ZX3气体溶于水呈碱性。W的外围电子排布是3s1。G2+离子的M层d轨道只有5个电子。请回答下列问题:
(1)W在元素周期表中的位置是 ;W和Z形成的化合物水溶液呈碱性,用离子方程式表示其原因 。
(2)Z原子的第一电离能比氧原子的 (填“大”或“小”);G的基态原子电子排布式是
(3)X与Y可形成多种化合物,其中一种化合物的分子式是X6Y6,分子中只有σ键,该分子的结构简式是 ;该化合物中Y的杂化轨道类型是 。
(4)G的最高价氧化物对应水化物的钾盐,在酸性条件下,常用于测定溶液中Fe2+的含量,该反应的离子方程式是
(5)可用YX4还原ZOx以消除其污染。已知:
YX4 (g) +4ZO2 (g)=4ZO(g)+YO2(g)+2X2O(g) △H= - 574 kJ·mol-1
YX4 (g)+4ZO(g)=2Z2 (g)十YO2 (g) +2X2O(g) △H = -1160 kJ·mol-1
试写出用YX4还原ZO2至Z2的热化学方程式___ _。
-
X、Y、Z、W、G是元素周期表中原子序数依次增大的五种元素。X元素是元素周期表中核电荷数最小的元素。Y的一种核素常用于考古,其一种同素异形体为自然界最硬的物质。ZX3气体溶于水呈碱性。W的外围电子排布是3s1。G2+离子的M层d轨道只有5个电子。请回答下列问题:
(1)W在元素周期表中的位置是______;W和Z形成的化合物水溶液呈碱性,用离子方程式表示其原因_____。
(2)Z原子的第一电离能比氧原子的____(填“大”或“小”);G的基态原子电子排布式是__________
(3)X与Y可形成多种化合物,其中一种化合物的分子式是X6Y6,分子中只有σ键,该分子的结构简式是_________;该化合物中Y的杂化轨道类型是________。
(4)G的最高价氧化物对应水化物的钾盐,在酸性条件下,常用于测定溶液中Fe2+的含量,该反应的离子方程式是____________
(5)可用YX4还原ZOx以消除其污染。已知:
YX4(g) +4ZO2(g)=4ZO(g)+YO2(g)+2X2O(g) △H=-574 kJ·mol-1
YX4(g)+4ZO(g)=2Z2(g)十YO2(g) +2X2O(g) △H = -1160kJ·mol-1
试写出用YX4还原ZO2至Z2的热化学方程式________。
-
短周期元素W、X、Y和Z的原子序数依次增大。其中W的原子半径最小,X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,且Y和Z可以形成化合物ZY2和ZY3。根据以上叙述,下列说法中正确的是
A.以上四种元素的原子半径大小为W<X<Y<Z
B.W、X、Y、Z原子的核外最外层电子数的总和为20
C.W与Y可形成既含极性共价键又含非极性共价键的化合物
D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点



