-
下表列出了两种燃煤烟气脱硫方法的原理.
方法Ⅰ:将 SO2 与 I2 反应制 H2SO4 和 HI,同时分解 HI 制 H2 和 I2,I2 循环使用。方法Ⅱ:用 Na2SO4 溶液吸收 SO2,再用离子膜电解法,电解吸收液得到单质硫。
(1)方法Ⅰ中,用 SO2 与碘反应生成 H2SO4 和 HI,SO2 与 I2 反应的物质的量之比为____________;制得的 H2 可用储氢合金转化为 MH,现分别用 NiO(OH)、MH 作正、负极材料,KOH 溶液作电解质,可制得高容量的镍氢电池.电池总反应为:NiO(OH)+MH Ni(OH)2+M 则电池放电时, 负极的电极反应式为_____________,充电完成时,Ni(OH)2 全部转化为 NiO (OH).若继续充电将在一个电极产生 O2,O2 扩散到另一电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极的电极反应式为____________________
Ni(OH)2+M 则电池放电时, 负极的电极反应式为_____________,充电完成时,Ni(OH)2 全部转化为 NiO (OH).若继续充电将在一个电极产生 O2,O2 扩散到另一电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极的电极反应式为____________________
(2)利用如图装置可实现方法Ⅱ的转化
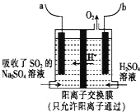
①b 端应连接电源的_____(填“正极”或“负极”).
②用 Na2SO4 溶液代替水吸收烟气中的 SO2 使之转化为 H2SO3,其目的是_____
③电解过程中,阴极的电极反应式为_____.
-
下表列出了3种燃煤烟气脱硫方法的原理。
| 方法Ⅰ | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
| 方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
| 方法Ⅲ | 用Na2SO3溶液吸收SO2,再经电解转化为H2SO4 |
(1)方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:
2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3
能提高燃煤烟气中SO2去除率的措施有________(填字母)。
A.增大氨水浓度
B.升高反应温度
C.使燃煤烟气与氨水充分接触
D.通入空气使HSO3-转化为SO42-
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是____________(用离子方程式表示)。
(2)方法Ⅱ中主要发生了下列反应:
2CO(g)+SO2(g)=S(g)+2CO2(g) ΔH=8.0 kJ·mol-1
2H2(g)+SO2(g)=S(g)+2H2O(g) ΔH=90.4 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH=-566.0 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1
S(g)与O2(g)反应生成SO2(g)的热化学方程式可表示为________。
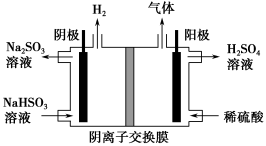
(3)方法Ⅲ中用惰性电极电解NaHSO3溶液的装置如下图所示。阳极区放出气体的成分为________(填化学式)。
-
下面是一种燃煤烟气脱硫方法的原理:用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。
其中氨水吸收燃煤烟气中SO2的化学反应为:
2NH3+SO2+H2O=(NH4)2SO3;(NH4)2SO3+SO2+H2O=2NH4HSO3
能提高燃煤烟气中SO2去除率的措施有________(填字母)。
①增大氨水浓度
②升高反应温度
③使燃煤烟气与氨水充分接触
④通入空气使HSO3-转化为SO42-
A.①② B.①②③④ C.①③ D.②③④
-
燃煤的烟气中含有SO2,为了治理雾霾天气,工厂采用多种方法实现烟气脱硫。
(1)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是______(填字母序号)。
a.石灰乳 b.CaCl2溶液
(2)某工厂利用含SO2的烟气处理含Cr2O72-的酸性废水,吸收塔中反应后的铬元素以Cr3+形式存在,具体流程如下:
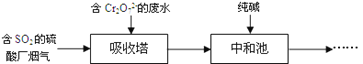
①用SO2处理含铬废水时,利用了SO2的______性。
②吸收塔中发生反应的离子方程式为____________________________________。
(3)该废水经处理后,测得有关数据如下(其他离子忽略不计):
| 离子 | Cr2O72- | Cr3+ | H + | Na + | SO42- |
| 浓度(mol/L) | a | 0.2×10-6 | 1.2×10-6 | 6.8×10-6 | 3.0×10-6 |
则a= ______。
-
研究燃煤烟气的脱硫(除SO2)和脱硝(除NOx)具有重要意义,请回答下列问题。
(1)采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NOx,获得(NH4)2SO4的稀溶液。已知常温下,该溶液的pH=5,则 =_________(该温度下NH3· H2O的Kb=1.7×10-5)。往(NH4)2SO4溶液中再加入少量(NH4)2SO4固体,
=_________(该温度下NH3· H2O的Kb=1.7×10-5)。往(NH4)2SO4溶液中再加入少量(NH4)2SO4固体, 的值将________(填“变大”、“不变”或“变小”)。
的值将________(填“变大”、“不变”或“变小”)。
(2)用乙烯作为还原剂将氮的氧化物还原为N2的脱硝技术,其脱硝机理示意图如下图1,脱硝率与温度,负载率(分子筛中催化剂的质量分数)的关系如图2所示。
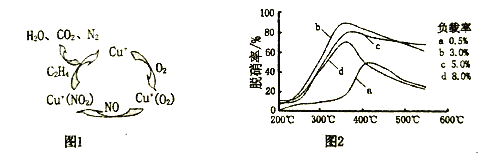
①写出该脱硝过程中乙烯和NO2反应的化学方程式:___________________。
②要达到最佳脱硝效果,应采取的条件是:___________________。
(3)利用如图装置可实现用Na2SO4溶液吸收SO2,再用离子膜电解法电解吸收液得到单质硫。

①a端应连接电源的_____(填“正极”或“负极”)。
②用Na2SO4溶液代替水吸收烟气中的SO2使之转化为H2SO3,其目的是_______________。
③电解过程中,阴极的电极反应式为______________。
-
煤炭是我国的主要能源之一,与之伴生的二氧化硫(SO2)和酸雨污染问题较为突出。目前我国采用的控制方法是电厂烟气脱硫。烟气脱硫的原理是利用碱性物质吸收并固定酸性的二氧化硫,主要有如下两种方法:
I、钠碱循环法脱硫技术。
(1)此法是利用Na2SO3溶液可脱除烟气中的SO2。Na2SO3可由NaOH溶液吸收SO2制得,该反应的离子方程式: 。
(2)NaOH溶液吸收SO的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
①由上表判断,NaHSO3溶液显 性,用化学平衡原理解释: 。
②当溶液呈中性时,离子浓度关系正确的是(选填字母): 。
a.c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H-)=c(OH-)
c.c(Na+)=2c(SO32-)+c(HSO3-)
II、石灰石脱硫法
此法是以石灰石为原料通过系列反应将硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g)△H=218.4kJ·mol-1(反应Ⅰ)
CaO(s)+SO2(g)+CO2(g)△H=218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g)△H2=-175.6kJ·mol-1(反应Ⅱ)
CaS(s)+4CO2(g)△H2=-175.6kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)结合反应Ⅰ、Ⅱ写出CaSO4(s)与CaS(s) 的热化学反应方程式 。
(2)对于气体参与的反应,表示平衡常数 Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅰ的Kp= (用表达式表示)。
(3)假设某温度下,反应Ⅰ的速率(v1)小于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是 。
(4)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中产生的SO2生成量的措施有 。
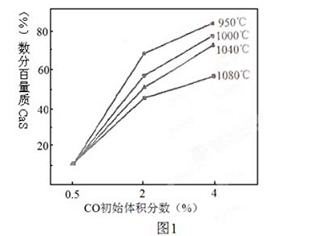
A、向该反应体系中投入生石灰
B、在合适的温度区间内控制较低的反应温度
C、降低CO的初始体积百分数
D、提高反应体系的温度
-
下列有关防止或减少酸雨的措施中不可行的是( )
A.对含SO2、NO2的废气处理后再排空
B.人工收集大气雷电产生的氮的氧化物
C.对燃煤及燃煤烟气进行脱硫
D.推广天然气、甲醇等作为汽车的燃料
-
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:
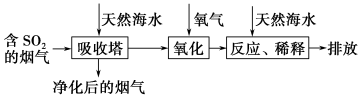
下列说法错误的是( )。
A.天然海水pH≈8的原因是海水中的CO32-、HCO3-水解
B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42-
C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸
D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同
-
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、CO32-、HCO3-、Br-等离子。火力发电燃煤排放的含有SO2的烟气可利用海水脱硫,其工艺流程如下所示:

下列说法错误的是:
A.含SO2的烟气若不经过海水脱硫直接排放可造成酸性降雨
B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42-
C.“反应、稀释”时加天然海水的目的是中和、稀释经氧化后海水中生成的酸
D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同
-
对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的.汽车尾气脱硝脱碳的主要原理为: 2NO(g)+2CO(g) N2(g)+2CO2(g)△H=akJ/mol
N2(g)+2CO2(g)△H=akJ/mol
I、已知2NO(g)+ O2(g)=2 NO2(g) △H =b kJ/mol;CO的燃烧热△H=c kJ/mol。写出消除汽车尾气中NO2的污染时,NO2与CO反应的热化学方程式________;
II、一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
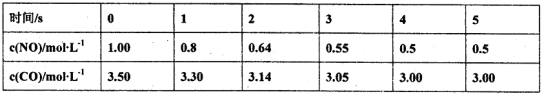
(1)在恒容密闭容器中充入CO、NO气体,下列图像正确且能说明反应达到平衡状态的是
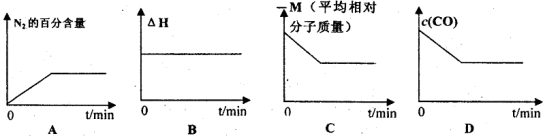
(2)前2s内的平均反应速率v(N2) = ________ mol/(L·s )(保留两位小数,下同);此温度下,该反应的平衡常数为________。
(3)采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NO2,获得(NH4)2SO4的稀溶液。
①常温条件下,此溶液的pH=5,则 = ________己知该温度下,NH3·H2O的Kb=1.7×10-5)
= ________己知该温度下,NH3·H2O的Kb=1.7×10-5)
②向此溶液中加入少量(NH4)2SO4固体, 的值将________(填“变大”、“不变”或“变小”)
的值将________(填“变大”、“不变”或“变小”)
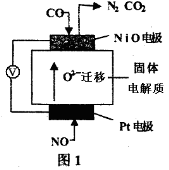
(4)设计如图1装置模拟传感器测定CO与NO反应原理。铂电极为________ (填“正极”或“负极”)。
Ni(OH)2+M 则电池放电时, 负极的电极反应式为_____________,充电完成时,Ni(OH)2 全部转化为 NiO (OH).若继续充电将在一个电极产生 O2,O2 扩散到另一电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极的电极反应式为____________________











