-
我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖。
(1)基态砷原子的价电子排布式为____。
(2)氟、氧、砷三种元素的电负性由大到小的顺序是____(用相应的元素符号填空)。
(3)Fe(SCN)3溶液中加人NH4F,发生如下反:Fe(SCN)3+6NH4F=== (NH4)3FeF6+3NH4SCN
①NH4F 中阳离子的立体构型为____。
②(NH4)3FeF6存在的微粒间作用力有__(选填序号,下同)。
a.离子键 b.共价键 c.金属键 d.配位键 e.范德华力 f.氢键
③已知SCN−中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为____,该原子团中σ与π键个数比为____。
(4)FeCl3晶体易溶于水、乙醇,受热易气化,而FeF3晶体熔点高于1000oC,试解释两种化合物熔点差异较大的原因:____。
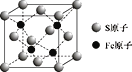
(5)S和Fe形成的某化合物,其晶胞如图所示,则该物质的化学式为 ___。设该晶胞的密度为ρ g/cm3,用NA表示阿伏加德罗常数,则该晶胞中距离最近的S原子之间的距离为(列出计算式即可)____cm。
-
我国化学家在“铁基(氟掺杂镨氧化铁砷合物)高温超导”材料研究上取得了重要成果,给研究项目荣获2013年度“国家自然科学奖”一等奖。
(1)Fe在周期表的位置为
(2)氟、氧、砷三种元素中电负性最小的是__________(用元素符号填空)。
(3)氧的最简单氢化物键角为 ,砷的最简单氢化物分子空间构型为 。
(4)FeCl3晶体易溶于水,乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因: 。
(5)铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如图。
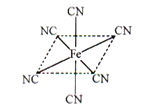
①已知CN-与N2结构相似,1molCN-中π键数目为 。
②上述沉淀溶解过程的化学式为
-
铁及铁的化合物在生活、生产中具有广泛应用,如亚铁氰化钾即K4[Fe(CN)6]是食盐中常用的抗结剂、铁基(氟掺杂镨氧铁砷化合物)是高温超导材料、“愚人金”是制备硫酸的主要矿物原料。请按要求回答下列问题。
(1)K4[Fe(CN)6]配合物中存在的作用力类型有__________________________(从“金属键”、“离子键”、“共价键”、“配位键”、“氢键”、“范德华力”中选填);其中CN-中各原子最外层均满足8电子稳定结构,其电子式为_____________,其中C原子的杂化形式是_________。
(2)铁基化合物中氟、氧、砷三种元素中电负性值由大到小的顺序是_____________(填元素符号)。其中氢化物(RH3)的某种性能(M)随R的核电荷数的变化趋势如图所示,则纵轴M可能表示为_____________________(从“沸点”、“稳定性”、“分子间作用力”、“R—H键能”中选填)。

(3)FeCl3晶体熔点为306℃,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因:____________________________________________。
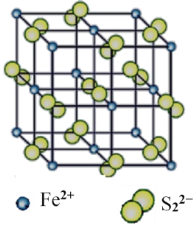
(4)“愚人金”是铁硫化合物,其晶体的晶胞如图所示。该晶体的化学式______________。
-
(12分)高温超导材料是科学家研究的重点物质之一。
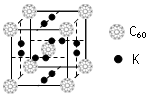
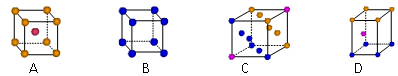
⑴科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如下左图所示。该富勒烯化合物中的K原子和C60分子的个数比为▲ 。

⑵某同学画出的C的核外电子排布(轨道表示式)如上右图所示,该电子排布图(轨道表示式)违背了▲ ,请你画出正确的电子排布图(轨道表示式)▲ 。
⑶金属钾采用的是下列▲ (填字母代号)堆积方式。
⑷富勒烯(C60)的结构如图。

①1 mol C60分子中σ键的数目为▲ 。
②已知:金刚石中的C-C的键长为154.45 pm,C60中C-C键长为145~140 pm。有同学据此推断C60的熔点高于金刚石,你认为是否正确并阐述理由:▲ 。
-
(12分)高温超导材料是科学家研究的重点物质之一。
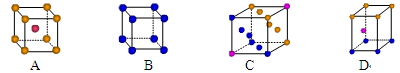
⑴科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如下左图所示。该富勒烯化合物中的化学式为。


⑵某同学画出的C的基态原子核外电子轨道表示式(如上右图),该电子排布图违背了________。
⑶金属钾采用的是下列________(填字母代号)堆积方式,每个钾原子的配位数是________
⑷富勒烯(C60)的结构如图。
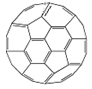
①1 mol C60分子中σ键的数目为________。
②已知:金刚石中的C-C的键长为154.45 pm,C60中C-C键长为145~140 pm。有同学据此推断C60的熔点高于金刚石,你认为是否正确并阐述理由:________。
-
数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果。在高温高压下CO具有极高的化学活性,能与多种单质或化合物反应。
(1)工业上常采用水蒸气喷到灼热的炭层上实现煤的气化(制得CO、H2),该反应的化学方程式是 。
(2)上述煤气化过程中需向炭层交替喷入空气和水蒸气,喷入空气的目的是 ;反应生成的气体在加热、催化剂作用条件下可合成液体燃料甲醇,该反应的化学方程式为 。
(3)一定条件下,CO与H2可合成甲烷,反应方程式为:CO(g)+3H2(g) CH4(g)+H2O (g)该条件下,该反应能够自发进行的原因是 。
CH4(g)+H2O (g)该条件下,该反应能够自发进行的原因是 。
(4)CO—空气燃料电池中使用的电解质是搀杂了Y2O3的ZrO2晶体,它在高温下能传导O2-。该电池正极的电极反应式为 。
(5)工业上可通过甲醇羰基化法制取甲酸甲酯,反应方程式为:
CH3OH(g)+CO(g) HCOOCH3(g) ΔH =-29.1 kJ·mol-1
HCOOCH3(g) ΔH =-29.1 kJ·mol-1
科研人员对该反应进行了研究,部分研究结果如下:
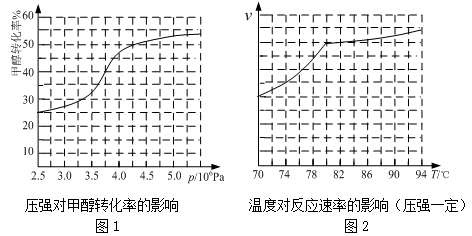
①根据反应体系的压强对甲醇转化率的影响并综合考虑生产成本因素,工业制取甲酸甲酯应选择的压强为 。
a.3.5×106Pa b.4.0×106Pa c.5.0×106Pa
②实际工业生产中采用的温度是 ,其理由是 。
-
我国是世界上研究超导技术比较先进的国家,在高温超导材料中,铊(81Tl)是重要成分之,已知铊和铝是同主族元素,关于铊的性质推断错误的是
A.铊是银白色,质软的金属
B.铊不能形成稳定的气态氢化物
C.铊与浓流酸反应生成 T12(SO4)3
D.Tl(OH)3是两性氢氧化物
-
在人们的印象中,塑料是常见的绝缘材料,但2000年三名诺贝尔化学奖得主的研究成果表明,塑料经改造后能像金属一样具有导电性,要使塑料聚合物导电,其内部的碳原子之间必须交替地以单键和双键结合(再经掺杂处理).目前导电聚合物已成为物理学家和化学家研究的重要领域.由上述分析,下列聚合物 经掺杂处理后可以制成“导电塑料”的是 ( )
A.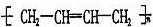 B.
B.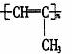
C.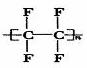 D.
D.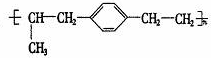
-
在人们的印象中,塑料是常见的绝缘材料,但2000年三名诺贝尔化学奖得主的研究成果表明,塑料经改造后能像金属一样具有导电性,要使塑料聚合物导电,其内部的碳原子之间必须交替地以单键和双键结合(再经掺杂处理)。目前导电聚合物已成为物理学家和化学家研究的重要领域.由上述分析,下列聚合物经掺杂处理后可以制成“导电塑料”的是 ( )
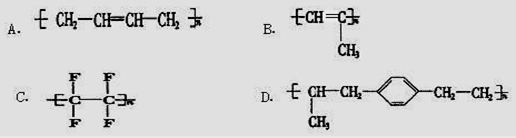
-
三位科学家因在烯烃复分解反应研究中的杰出贡献而荣获2005年度诺贝尔化学奖,烯烃复分解反应可示意如下:

下列化合物中,经过烯烃复分解反应可以生成 的是
的是
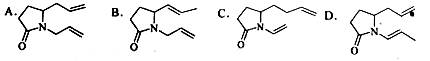











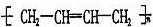 B.
B.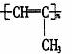
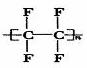 D.
D.


