已知热化学方程式:2SO2(g)+O2(g)2SO3(g) △H=―196.64kJ/mol。在容器中充入1molSO2和0.5molO2充分反应,最终放出的热量为
A. 98.32kJ B. 98.32kJ/mol C. <98.32kJ D. >98.32kJ
高二化学单选题简单题
已知热化学方程式:2SO2(g)+O2(g)2SO3(g) △H=―196.64kJ/mol。在容器中充入1molSO2和0.5molO2充分反应,最终放出的热量为
A. 98.32kJ B. 98.32kJ/mol C. <98.32kJ D. >98.32kJ
高二化学单选题简单题
已知热化学方程式:2SO2(g)+O2(g)2SO3(g) △H=―196.64kJ/mol。在容器中充入1molSO2和0.5molO2充分反应,最终放出的热量为
A. 98.32kJ B. 98.32kJ/mol C. <98.32kJ D. >98.32kJ
高二化学单选题简单题查看答案及解析
已知热化学方程式:2SO2(g)+ O2(g) 2SO3(g) △H = ―196.64kJ/mol
在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为 ( )。
A . 196.64kJ B. 196.64kJ/mol C. < 196.64kJ D. > 196.64kJ
高二化学选择题简单题查看答案及解析
已知2SO2(g)+O2(g) 2SO3(g);△H= -197kJ/mol,同温下,往相同体积的密闭容器甲、乙中分别充入2molSO2、1molO2 和1molSO3、1molSO2、0.5molO2,当它们分别达到平衡时放出的热量为Q1KJ和Q2KJ,则下列比较正确的是
A.Q2=1/2Q1=98.5 B.Q2=1/2Q1<98.5 C.Q2<1/2Q1<98.5 D.无法确定
高二化学选择题简单题查看答案及解析
已知2SO2(g)+O2(g)2SO3(g) ΔH=-197kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲)2molSO2和1molO2;(乙)1molSO2和0.5molO2;(丙)2mol O3。恒温、恒容下反应达平衡时,下列关系一定正确的是( )
A.容器内压强P:P甲=P丙>2P乙
B.反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
C.c(SO2)与c(O2)之比k:k甲=k丙>k乙
D.SO3的质量m:m甲=m丙>2m乙
高二化学单选题困难题查看答案及解析
实验室测得4 mol SO2发生下列化学反应:2SO2(g)+O2(g)2SO3(g) ΔH=-196.64 kJ/mol。当放出314.3 kJ热量时,SO2转化率最接近于( )。
A.40% B.50% C.80% D.90%
高二化学选择题简单题查看答案及解析
(14分)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
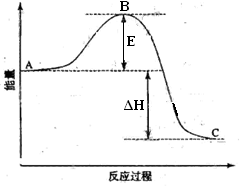
(1)图中A、C分别表示________、________,E的大小对该反应的反应热________(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点________(填“升高”还是“降低”),△H________(填“变大”、“变小”或“不变”),理由是________
(2)图中△H=________KJ·mol-1
高二化学填空题中等难度题查看答案及解析
(I)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。
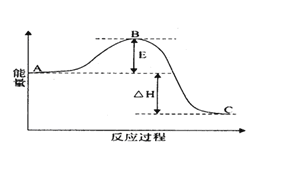
已知1molSO2(g)氧化为1molSO3(g)的△H=-99kJ•mol-1.请回答下列问题:
(1)E的大小对该反应的反应热______(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点______(填“升高”还是“降低”)。
(2)完成SO2氧化为SO3的热化学方程式______________________。
(II)用 50mL0.50mol/L 盐酸与 50mL0.55mol/LNaOH 溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
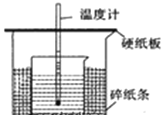
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________。实验中能否用环形铜丝搅拌棒代替该用品_______(填“能”或“否”)
(2)向盐酸溶液中加入NaOH溶液的正确操作是_______(从下列选出)。
A.沿玻璃棒缓慢倒入 B. —次迅速倒入 C.分三次少量倒入
(3)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会_____(填“偏大”、“偏小”、“无影响”)。
(4)小明利用上述装置做实验,测得中和热的数值偏低,请你分析可能的原因是__________________。
A.测量完盐酸的温度再次测最NaOH溶液温度时,温度计上残留的酸液未用水冲洗干净。
B.做本实验的当天室温较高 C.大小烧杯口不平齐,小烧杯口未接触硬纸板。
D.在量取盐酸时仰视读数 E.大烧杯的盖板中间小孔太大
高二化学综合题中等难度题查看答案及解析
已知2SO2(g)+O2(g)
2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1mol SO3(g)的ΔH= —99kJ/mol。
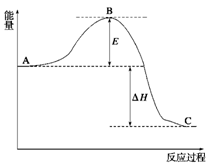
请回答下列问题:
(1)图中A点表示: ;图中C点表示: ;
(2)写出 SO3(g)分解成SO2(g)和O2(g)的热化学方程式 ;
(3)能量E在一定条件下可以降低,这种条件是: ;
(4)SO3溶于水可生成H2SO4 ,化学方程式为 ;
高二化学填空题中等难度题查看答案及解析
(12分)2SO2(g)+ O2 (g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1molSO3(g)的ΔH = -99 kJ·mol-1
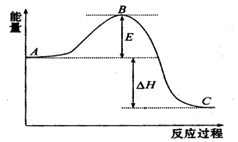
请回答下列问题:
(1)图中A表示 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? 加入V2O5后,上述反应ΔH (填变大、不变、变小)
(2)图中ΔH = kJ·mol-1。
(3)如果反应速率v(SO2)为0.06 mol·L-1·min-1,则v(O2)为 mol·L-1·min-1。
(4)已知S(s) + O2(g) = SO2(g) ΔH = -296 kJ·mol-1,则由S(s)生成5 mol SO3(g)的ΔH= kJ·mol-1。
高二化学填空题困难题查看答案及解析
实验室用4 mol SO2与2 mol O2在一定条件下进行下列反应:2SO2(g)+O2(g)==2SO3(g)ΔH=-196.64 kJ/mol,当放出314.624 kJ热量时,SO2的转化率为( )
A.40% B.50% C.80% D.90%
高二化学选择题中等难度题查看答案及解析