-
已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=-452 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
A. 1molCO 完全燃烧,放出热量为283 J
B. Na2O2(s)+CO2(s)=Na2CO3(s)+  O2(g) △H=-226 kJ·mol-l
O2(g) △H=-226 kJ·mol-l
C. CO(g) 与Na2O2(s)反应放出509kJ 热量时,电子转移数为1.204×1024
D. CO 的燃烧热为566 kJ·mol-1
-
已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=-452 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
A. 1molCO 完全燃烧,放出热量为283 J
B. Na2O2(s)+CO2(s)=Na2CO3(s)+  O2(g) △H=-226 kJ·mol-l
O2(g) △H=-226 kJ·mol-l
C. CO(g) 与Na2O2(s)反应放出509kJ 热量时,电子转移数为1.204×1024
D. CO 的燃烧热为566 kJ·mol-1
-
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) ΔH=-452 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
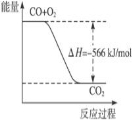
A.右图可表示由CO生成CO2的反应过程和能量关系
B.CO的燃烧热为566 kJ/mol
C.Na2O2(s)+CO2(s)=Na2CO3(s)+1/2O2(g) ΔH=-226 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2×6.02×1023
-
已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol,Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g);△H=-226kJ/mol根据以上热化学方程式判断,下列说法正确的是( )
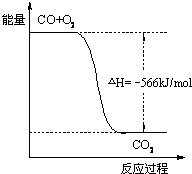
A.CO的燃烧热为283 kJ
B.如图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g);△H>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
-
已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol,Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g);△H=-226kJ/mol根据以上热化学方程式判断,下列说法正确的是( )
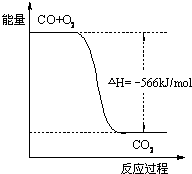
A.CO的燃烧热为283 kJ
B.如图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g);△H>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
-
已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol,Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g);△H=-226kJ/mol根据以上热化学方程式判断,下列说法正确的是( )
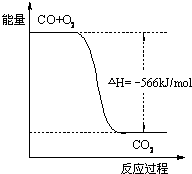
A.CO的燃烧热为283 kJ
B.如图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g);△H>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
-
(12分)为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·moL-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6KJ·moL-1
H2O (g)=H2O(l) ΔH=-44.0KJ·moL-1
(1)氢气的燃烧热△H= 。
(2)写出CO和H2O(g)作用生成CO2和H2的热化学方程式 。
(3)往1L体积不变的容器中加入1.00mol CO和1.00mol H2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO 的转化率为 ;反应达到平衡后,升高温度,此时平衡常数将 (填“变大”、“不变”或“变小”),平衡将向 (填“正”或“逆”)反应方向移动。
(4)为了提高CO的转化率,可采取的措施是 。
A.增大的CO浓度 B.增大H2O(g) 的浓度
C.使用催化剂 D.降低温度
(5)H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以氢氧化钾为电解质溶液,其负极的电极反应式是 。
-
为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2.已知:
2CO(g)+O2(g)=2CO2(g)△H=-566kJ•moL-1
2H2(g)+O2(g)=2H2O(g)△H=-483.6KJ•moL-1
H2O (g)=H2O(l)△H=-44.0KJ•moL-1
(1)氢气的标准燃烧热△H=________kJ•moL-1
(2)写出CO和H2O(g)作用生成CO2和H2的热化学方程式________
(3)往 1L体积不变的容器中加入1.00mol CO和1.00mol H2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为________;反应达到平衡后,升高温度,此时平衡常数将________(填“变大”、“不变”或“变小”),平衡将向________ (填“正”或“逆”)方向移动
(4)为了提高CO的转化率,可采取的措施是________.
A.增大的CO浓度 B.增大的H2O(g)浓度 C.使用催化剂 D.降低温度
(5)H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以KOH为电解质溶液,其负极的电极反应式是________.
-
氮和硫的化合物在生产生活中广泛存在。研究发现,NOx和SO2是雾霾的主要成分。
Ⅰ.(1)已知:
2CO(g)+O2(g)  2CO2(g) △H1=﹣566.00kJ•mol-1
2CO2(g) △H1=﹣566.00kJ•mol-1
2SO2(g)+O2(g)  2SO3(g) △H2=﹣196.6kJ•mol-1
2SO3(g) △H2=﹣196.6kJ•mol-1
2NO(g)+O2(g)  2NO2(g) △H3=﹣113.0kJ•mol-1
2NO2(g) △H3=﹣113.0kJ•mol-1
则反应2NO2(g)+SO2(g)+ CO(g)  SO3(g)+2NO(g)+ CO2(g)的△H=_________kJ•mol-1。
SO3(g)+2NO(g)+ CO2(g)的△H=_________kJ•mol-1。
(2)NOx主要来源于汽车尾气。T℃时,模拟汽车尾气催化转化:2NO+2CO 2CO2+N2,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化如右图所示:
2CO2+N2,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化如右图所示:

①T℃时该化学反应的平衡常数K=____;
②图中a、b分别表示使用同种催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是____(填“a”或“b”)。
Ⅱ.科学家发明了NH3燃料电池,以KOH为电解质,原理如右图所示。该燃料电池的负极反应式为__________________。

Ⅲ.SO2主要来源于煤的燃烧。
25℃时,电离平衡常数:
| 化学式 | H2CO3 | H2SO3 |
| 电离平衡常数 | K1=4.30×10-7 K2=5.61×10-11 | K1=1.54×10-2 K2=1.02×10-7 |
回答下列问题:
(1)常温下,pH相同的下列溶液:①Na2CO3、②NaHCO3、③Na2SO3。物质的量浓度由大到小的排列顺序为___________>___________>___________。(用序号表示)
(2)已知NaHSO3溶液显酸性,下列说法正确的是_________________。
A. c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3)
B. c(Na+)+c(H+)=c(OH-)+c(HSO3-)+c(SO32-)
C. c(HSO3-)> c(H+)> c(H2SO3)> c(SO32-)
D. c(H+)+c(H2SO3)=c(SO32-)+c(OH-)
-
(17分) 为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:
2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·moL-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6KJ·moL-1
H2O (g)=H2O(l) ΔH=-44.0KJ·moL-1
(1)氢气的标准燃烧热△H= kJ·moL-1
(2)写出CO和H2O(g)作用生成CO2和H2的热化学方程式
(3)往 1L体积不变的容器中加入1.00mol CO和1.00mol H2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO 的转化率为 ;反应达到平衡后,升高温度,此时平衡常数将 (填“变大”、“不变”或“变小”),平衡将向________ (填“正”或“逆”)方向移动
(4)为了提高CO的转化率,可采取的措施是 。
A.增大的CO浓度 B.增大的H2O(g)浓度 C.使用催化剂 D.降低温度
(5)H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以KOH为电解质溶液,其负极的电极反应式是
O2(g) △H=-226 kJ·mol-l





