-
1 L水中溶有Mg(HCO3)2和CaCl2的浓度分别是b mol·L-1和2b mol·L-1,现用一种试剂(适量)把Ca2+、Mg2+除去,这种试剂最好选用 ( )。
A.Ca(OH)2 B.NaOH C.NaHCO3 D.Na2CO3
高二化学选择题中等难度题查看答案及解析
-
1 L水中溶有Mg(HCO3)2和CaCl2的浓度分别是b mol/L和2b mol/L,现用一种试剂(适量)把Ca2+、Mg2+除去,这种试剂最好选用( )
A.Ca(OH)2 B.NaOH
C.NaHCO3 D.Na2CO3]
高二化学选择题中等难度题查看答案及解析
-
在浓度为0.01mol/L Mg(HCO3)2,0.02mol/LCaCl2的水溶液1L中,要同时除去Mg2+,Ca2+应选用的试剂是( )
A. NaHCO3 B. Na2CO3 C. Ca(OH)2 D. NaOH
高二化学选择题简单题查看答案及解析
-
已知25℃时,CaCO3饱和溶液中c(Ca2+)为5.3×10-5mol/L、MgCO3的饱和溶液中c(Mg2+)为2.6×10-3mol/L.若在5mL浓度均为0.01mol/L的CaCl2和MgCl2溶液中,逐滴加入5mL 0.012mol/LNa2CO3溶液,充分反应后过滤得到溶液M和沉淀N(不考虑溶液体积的变化)。下列观点不正确的是
A. 25℃时,Ksp(CaCO3)=2.8×10-9
B. 加入Na2CO3溶液的过程中,先生成CaCO3沉淀
C. 滤液M中:c(Cl-)>c(Na+)>c(Mg2+)>c(CO3-)>c(OH-)
D. 滤液M中:
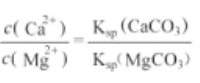
高二化学单选题困难题查看答案及解析
-
海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
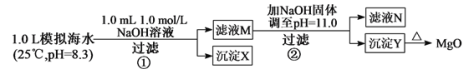
模拟海水中的离
子浓度(mol/L)
Na+
Mg2+
Ca2+
Cl−
HCO3-
0.439
0.050
0.011
0.560
0.001
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。
下列说法正确的是
A. 步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
B. 滤液M中存在Mg2+,不存在Ca2+
C. 滤液N中存在Mg2+、Ca2+
D. 沉淀物X为CaCO3
高二化学单选题中等难度题查看答案及解析
-
除去NaCl中含有的Ca2+、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④HCl。加入试剂合理的操作顺序是 ( )
A.①②③④ B.③①②④ C.④②①③ D.③②①④
高二化学选择题中等难度题查看答案及解析
-
除去NaCl中含有的Ca2+、Mg2+、SO42-、HCO3-等离子通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④HCl。加入试剂合理的操作顺序是
A.①②③④ B.③①②④ C.④②①③ D.③②①④
高二化学选择题中等难度题查看答案及解析
-
下列离子方程式错误的是
A.氯气通入水中:C12 + H2O
H+ + C1-+ HClO
B.向Mg(HCO3)2溶液中加入过量的澄清石灰水:
Mg2++2HCO3—+2OH一+Ca2+ MgCO3+CaCO3↓+2H2O.
C.将适量的CO2通入Ca(C1O)2溶液中:
Ca2++2C1O—+CO2+H2O 2HC1O+CaCO3↓
D.Ba(OH)2溶液中加入过量的Al2(SO4)3溶液:
3Ba2++6OH—+2Al3++3SO42— 3BaSO4↓+2Al(OH)3↓
高二化学选择题中等难度题查看答案及解析
-
某城市用水中含c(Ca2+)为1.0×10-3 mol·L-1,c(Mg2+)为5.0×10-4 mol·L-1,c(HCO3-)为8.0×10-4 mol·L-1。如用药剂软化该水1 000 L,应加入Ca(OH)2________g,Na2CO3________g;如果水中含Mg2+,加入Na2CO3后,为尽量减少水中的Mg2+的浓度,可将水加热至沸,加热时反应的化学方程式为________。
高二化学填空题简单题查看答案及解析
-
(10分)某海域海水一些化学成分如下表
海水成分
Na+
Ca2+
Mg2+
HCO3-
Zn2+
含量/mol·L-1
0.4
0.002
0.045
0.002
10-7
已知:25℃时,Ksp(CaCO3)=2.8×10-9、Ksp(MgCO3)=6.8×10-6,Ksp[Mg(OH)2]=1.8×10-11。
某化学小组同学欲在实验制备MgCl2,并提取Zn。设计流程如下:

[假设①②过程溶液体积不变,忽略分离过程的损失]
(1)25℃时测得海水的pH为8.0,其原因是(写离子方程式) 。
(2)下图为溶液pH与对应的Zn2+、[Zn(OH)4]2-物质的量浓度的对数坐标图。

请结合图中数据回答:
试剂X的化学式为 ;由滤液F到沉淀C过程(一般认为离子浓度低于10-5mol/L就是沉淀完全),则调节的pH的范围为 。
(3)同学们发现,把MgCl2溶液蒸发、灼烧所得的白色固体难溶解于水,于是认为其主要成分是MgO。你认为 (填“正确”、“不正确”),原因是(用化学方程式表示) 、 。
(4)由图中c(Zn2+)计算Zn(OH)2的溶度积Ksp= 。
高二化学填空题困难题查看答案及解析