-
I.A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。A为_____,B为_____,C为_____,D的最高价氧化物的水化物是_____。 (用化学式填空)
Ⅱ.一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
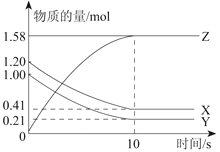
(1)反应开始到10 s,用Z表示的反应速率为_______________mol/(L•s)。
(2)反应开始到10 s,X的物质的量浓度减少了____________mol/L。
(3)反应的化学方程式为:______________________________。
-
A、B、C、D、E、F均为前四周期的元素,原子序数依次增大,A的核外电子数等于其电子层数,B的最外层电子数是次外层电子数的3倍,A和C、B和E同主族,B、C、D的离子具有相同的电子层结构,D的离子是同周期中离子半径最小的,F原子中共有6个未成对电子.
请回答下列问题:
(1)写出下列元素的元素符号:A______、C______、E______、F______.
(2)元素A和元素B可以形成A2B物质甲,写出甲的分子式______,甲为______(填“极性”或“非极性”)分子.
(3)元素A和元素E形成化合物乙,用电子式表示化合物乙______;常温下甲为液态,乙为气态,试解释原因______.
(4)元素A与元素C形成化合物丙,丙的水溶液显碱性,试用化学方程式解释其原因:______.
(5)元素C、元素D的最高价氧化物的水化物相互反应的离子方程式是______.
(6)写出元素F的外围电子排布式______.
-
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是 ( )
A. R的原子半径比Z的大 B. R的氢化物的热稳定性比W的强
C. X与Y形成的化合物只有一种 D. Y的最高价氧化物的水化物的酸性比W的强
-
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是 ( )
A. R的原子半径比Z的大
B. Y的最高价氧化物的水化物的酸性比W的强
C. X与Y形成的化合物只有一种
D. R的氢化物的热稳定性比W的强
-
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是( )
A.R的原子半径比Z的大
B.R的氢化物的热稳定性比W的强
C.X与Y形成的化合物只有一种
D.Y的最高价氧化物的水化物的酸性比W的强
-
五种短周期元素A、B、C、D、E、F的原子序数依次增大.A和C同族,B和E同族,C离子和B离子具有相同的电子层结构,D的最外层电子数与电子层数相同.A和B、E、F均能形成共价化合物(由分子构成的化合物).A和B形成的化合物在水中呈碱性,C和F形成的化合物在水中呈中性.
回答下列问题:
(1)五种元素中,原子半径最大的是______(填元素名称).最高价氧化物对应水化物酸性最强的元素为____ (填元素符号),其最高价氧化物对应水化物与NaOH反应的离子方程式为___________________________.
(2)由A和B、E、F所形成的化合物中,热稳定性最差的是_________________ (用化学式表示).
(3)A和F形成的化合物与A和B形成的化合物反应,产物的化学式为________.
(4)D元素最高价氧化物的化学式为_______,最高价氧化物对应水化物与氢氧化钠反应的离子方程式为___________________________.
(5)单质F与水反应的离子方程式为___________________..
-
A、B、C、D、E分别代表五种短周期元素,且原子序数依次增大,已知:B的最外层电子排布是nsnnpn+1;C的p能级上未成对的电子比B少一个;D的二价阳离子与C的阴离子具有相同的电子层结构;E与D同周期且E在该周期中原子半径最小;B与A的单质能生成具有刺激性气味的气体,该气体极易溶于水.
(1)B原子核外电子排布式为______.
(2)A与E化合时原子间以______键相结合,D与C化合时原子间以______键相结合.
(3)写出A、C的单质直接化合形成的化合物与E单质反应的离子方程式:______.
(4)A与B形成化合物时,中心原子采取______杂化成键,其立体结构为______,属于______(填“极性”或“非极性”)分子.
(5)将白色的无水CuSO4溶解于A2C中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子.请写出生成此配合离子的离子方程式:______.
(6)五种元素中电负性最大的是______(填元素名称).
-
短周期主族元素m、n、p、q的原子序数依次增大,它们的最外层电子数之和为18,n3-与p2+具有相同的电子层结构。下列叙述错误的是 ( )
A.m、n、q一定均是非金属元素
B.离子半径的大小:q>n>p
C.最高价氧化物对应水化物的酸性:q>n>m
D.m、n、p分别与q形成的二元化合物均含有共价键
-
A、B、C、D、E分别代表五种短周期元素,且原子序数依次增大,已知:B的最外层电子排布是ns2npn+1;C的p能级上未成对的电子比B少一个;D的二价阳离子与C的阴离子具有相同的电子层结构;E与D同周期且E在该周期中原子半径最小;B与A的单质能生成具有刺激性气味的气体。
(1)B原子核外电子排布式为___。
(2)A与E化合时原子间以___键相结合,D与C化合时原子间以___键相结合。
(3)写出A、C的单质直接化合形成的化合物与E单质反应的离子方程式为___。
(4)A与B形成化合物时,中心原子采取___杂化方式成键,其立体构型为___,属于___(填“极性”或“非极性”)分子。
-
(14分)A、B、C、D、E、F均为前四周期的元素,原子序数依次增大,A的核外电子数等于其电子层数,B的最外层电子数是次外层电子数的3倍,A和C、B和E同主族,B、C、D的离子具有相同的电子层结构,D的离子是同周期中离子半径最小的,F原子中共有6个未成对电子。
请回答下列问题:
⑴写出下列元素的元素符号:A ▲ 、C▲ 、E▲ 、F▲ 。
⑵元素A和元素B可以形成A2B物质甲,写出甲的分子式▲ ,甲为▲ (填“极性”或“非极性”)分子。
⑶元素A和元素E形成化合物乙,用电子式表示化合物乙▲ ;常温下甲为液态,乙为气态,试解释原因▲ 。
⑷元素A与元素C形成化合物丙,丙的水溶液显碱性,试用化学方程式解释其原因:
▲ 。
⑸元素C、元素D的最高价氧化物的水化物相互反应的离子方程式是▲ 。
⑹写出元素F的外围电子排布式▲ 。
