-
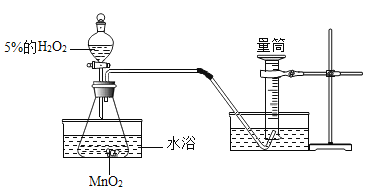
某化学兴趣小组为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置,进行了两次实验,两次实验的部分设计如表所示:
| 实验1 | 实验2 |
| MnO2的质量/克 | 0.5 | 0.5 |
| 5%的H2O2体积/毫升 | 40 | 待填 |
| 水浴温度/℃ | 20 | 80 |
温馨提示:本实验中的“水浴”是指通过水槽中的热水把热量传递到需要加热的锥形瓶里,达到加热的目的。
(1)该实验中收集气体的方法叫_____。
(2)实验2中“待填”的数据应为_____。
(3)实验结束后若要将MnO2从混合物中分离出来,可采取如下操作:_____、洗涤、干燥。
(4)在两次实验中,可通过_____来比较H2O2分解反应速率的大小。
(5)下列有关该实验的说法不正确的是_____。(填序号)
A 若俯视读数,则会导致测得的气体体积偏大
B 锥形瓶中原有的空气进入量筒会导致测得的气体体积偏大
C 实验过程中需待气泡连续且均匀产生时才能将导管伸到量筒口进行收集气体测定体积
D 实验2中由于温度较高使气体受热膨胀,会导致测得的分解速率比实际快
-
小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:

(1)写出实验中发生的化学反应的化学式表达式:_____________,二氧化锰在反应中的作用是__________。取用二氧化锰可以用________(填“药匙”或“镊子”)。
(2)MnO2中锰元素的化合价为___________;
(3)实验2中应加入5%H2O2_____________毫升;
(4)在两次实验中,可通过_______________来比较H2O2分解反应速率的大小;
(5)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有______________;
(6)实验结束后若要将MnO2从混合物中分离回收,可采取的方法是_____________。该方法用到的玻璃仪器有玻璃棒、___________、____________。玻璃棒的作用是______,将本实验中的二氧化锰经分离、干燥后称量,其质量为________g。
-
小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
| 实验1 | 实验2 |
| MnO2的质量/克 | 0.5 | 0.5 |
| 5%的H2O2的体积/毫升 | 40 | 待填 |
| 水浴温度/℃ | 20 | 80 |
(1)实验2中应加入5%H2O2 毫升。
(2)在两次实验中,可通过 来比较H2O2分解反应速率的大小。
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有 。
(4)实验结束后若要将MnO2从混合物汇总分离出来,可采取的方法是 。
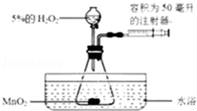
-
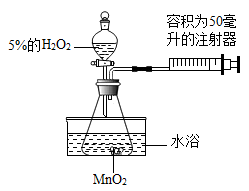
小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置去),进行了两次实验,两次实验的部分设计如表所示:
| 实验1 | 实验2 |
| MnO2的质量/克 | 0.5 | 0.5 |
| 5%的H2O2的体积/毫升 | 40 | 待填 |
| 水浴温度/℃ | 20 | 80 |
(1)实验2中应加入5%H2O2 毫升;
(2)在两次实验中,可通过观察 来比较H2O2分解反应速率的大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有 ;
(4)实验结束后若要将MnO2从混合物中分离出来,可采取的实验操作方法是1 、2洗涤、3干燥.
-
实验室常用过氧化氢溶液和二氧化锰制氧气,回答下列问题:
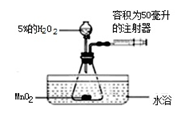
(1)为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置)去),进行了两次实验,两次实验的部分设计如表所示:
| 实验1 | 实验2 |
| MnO2的质量 | 0.5克 | 0.5克 |
| 5%的H2O2溶液体积 | 40mL | 待填 |
| 水浴温度 | 20℃ | 80℃ |
① 此反应的符号表达式是______________
② 实验2中“待填”的数据是 毫升;在两次实验中,可以通过一定时间内__________内的______________的多少来精确比较H2O2分解反应速率的大小。
③ 实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还可能的原因有 。
④ 实验结束后若要将不溶于水的MnO2从剩余物中分离出来,实验操作步骤(简单描述)是___________→用水冲洗MnO2 →烘干二氧化锰。
(2)探究使带火星木条复燃的氧气的最低浓度。用容积为300mL的集气瓶排水法收集氧气,当刚好把瓶中预先留有的100mL水排尽时,集气瓶中氧气的体积分数为(写出计算式即可):________________________。
实验研究结果显示:O2的体积分数大于49%时就可使带火星的木条复燃。因此,用带火星的木条验满O 2的方法 (填“可靠”或“不可靠”)。为此,收集O2时最好使用 集气法(不需要验满)。
-
资料显示,将新制的浓度为5%的H2O2溶液加热到80℃时,才有较多氧气产生。小红为了探究温度对H2O2分解反应速率的影响,借助下图所示实验装置(加持装置略去),进行了两次实验,两次实验的部分设计如下表所示:
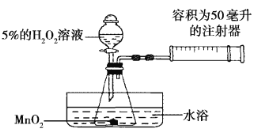
| 实验1 | 实验2 |
| MnO2 | 0.5 | 0.5 |
| 5%的H2O2溶液的体积/毫升 | 40 | 待填 |
| 水浴温度/ C C | 20 | 80 |
| | |
(1)①写出实验中发生化学反应的符号表达式___________,基本反应类型是___________。
②实验2中应加入5%H2O2溶液__________毫升。
③在两次实验中,可通过_________来比较H2O2溶液分解反应速率的大小。
④实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有______________。
(2)实验探究:如图所示,向三支试管中分别滴加浓度相同的三种溶液,观察可见:实验①中无明显现象,实验②中产生气泡,实验③中产生气泡更快,据悉你能得出的结论是________________。
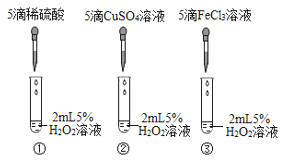
-
南开中学的牛小政同学为了探究温度对过氧化氢分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
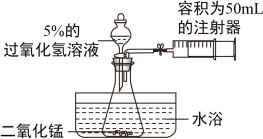
| 实验1 | 实验2 |
| 二氧化锰质量/g | 0.5 | 0.5 |
| 5%的过氧化氢溶液/mL | 40 | 待填 |
| 水浴温度/°C | 20 | 80 |
(1)写出该反应涉及的化学方程式:___________,其中二氧化锰的作用是______。
(2)实验2中应加入5%过氧化氢溶液____________mL。
(3)在两次实验中,可通过___________来比较过氧化氢分解反应速率的大小。
-
某校化学实验小组的同学们对影响化学反应速率的因素产生了兴趣,为了探究氧化铁能否加快过氧化氢的分解,他们设计了实验装置,并进行气体的制备和测量实验。实验时均以生成40mL气体为标准,相关实验数据记录如表:
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 过氧化氢溶液温度/℃ | 氧化铁的用量/g | 收集40mL氧气所需时间/s |
| ① | 5 | 10 | 20 | 0 | 128.5 |
| ② | 5 | 10 | 20 | 1.2 | 16.8 |
| ③ | 15 | 10 | 20 | 1.2 | 10.5 |
| ④ | 5 | 10 | 70 | 0 | 32.7 |
(1)若要证明氧化铁是过氧化氢分解的催化剂,还需要验证它在该反应前后质量和_____未发生改变。请写出过氧化氢在氧化铁的催化下反应的文字表达式:_____,该反应属_____反应(填基本反应类型)
(2)完成上述实验及数据的测定需要用到如图1中的部分装置,请按组装顺序写出所用到的装置代号_____。
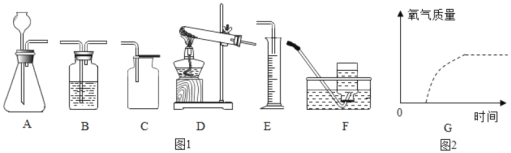
(3)用一定量10%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总量_____(选填“减小”“不变”或“增大”)。
(4)通过实验①和④对比可知,温度越高化学反应速率越快,同理通过实验②和③对比可知,得出结论是_____。
查阅资料:将新制的溶质质量分数为5%的过氧化氢溶液,加热到80℃时,才有较多氧气产生,而相同质量5%的过氧化氢溶液加入催化剂,常温下就会立即产生氧气。
(5)采用相同质量5%的过氧化氢溶液,图G虚线表示加热分解制取氧气的曲线,请你在该图2中用实线画出利用催化剂制取氧气的大致曲线(假定两种方法过氧化氢均完全分解)。_________
(6)同学们还想探究催化剂的颗粒大小对化学反应速率是否有影响,请你帮他们设计实验方案进行探究。___________
-
(8分)某化学兴趣小组在学习氧气的制法后进行一系列探究活动。
探究1.
利用如图实验装置制取氧气。

(1)写出用A装置制取氧气的化学方程式 。
探究2.
(2)小组对过氧化氢分解时影响反应速率的部分因素作出探究,并测得相关实验数据。如表:
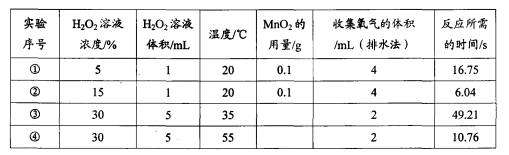
从实验③和④对比可知,化学反应速率与 有关。通过实验 与实验 (填实验序号)对比可知,化学反应速率与反应物的浓度有关。若用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,加适量水稀释,产生氧气的总质量 。(选填“减小”或“不变”或“增大”)。
探究3.
小组中小童同学取15%的H2O2溶液5mL于试管中,加热后,观察到溶液中产生较多气泡,他直接将带火星的木条伸入试管中,木条却没有复燃,直至溶液沸腾,也未见木条复燃。小组一起反复实验讨论并通过查找资料找到了木条不能复燃的原因。
(3)有关小童在实验中带火星的木条没有复燃,下列说法中正确的有 。
A.实验所用的过氧化氢溶液的浓度太小。
B.加热过氧化氢能分解,但反应速率较慢,试管中氧气含量较少。
C.加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,木条不能复燃。
D.小童采用排水法去收集产生的气体,再用带火星木条检验,木条能复燃。
-
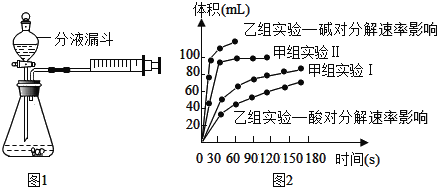
现甲、乙两化学小组安装两套如图1相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
(1)写出上述反应的化学方程式为_____。
(2)甲、乙小组设计如下实验设计方案。
| 实验编号 | 温度 | 等质量的催化剂 | 浓度 |
| 甲组实验I | 25℃ | 0.5g二氧化锰 | 10mL3.49%H2O2 |
| 甲组实验Ⅱ | 25℃ | 0.5g二氧化锰 | 10mL6.8%H2O2 |
| 实验编号 | 温度 | 等质量的催化剂 | 浓度 | 加入等浓度的试剂(各2mL) |
| 乙组实验I | 25℃ | 0.5g二氧化锰 | 10mL6.8%H2O2 | 氢氧化钠 |
| 乙组实验Ⅱ | 25℃ | 0.5g二氧化锰 | 10mL68%H2O2 | 硫酸 |
最终实验得到的结果如图2所示,回答下列问题:
①通过甲组实验得出的数据分析,得到的结论是_____;
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析:相同条件下,H2O2在_____(填“酸”或“碱”)性环境下放出气体速率较快。
(3)下列有关H2O2溶液,说法中不正确的是(____)
A H2O2溶液是混合物
B 5.1%的H2O2溶液中氢元素的质量分数为0.3%
C 二氧化锰并不是H2O2分解唯一的催化剂
D H2O2中氢分子和氧分子的个数比为1:1
(4)医学上常用过氧化氢溶液来清洗创口和局部抗菌。为了测定一瓶医用过氧化氢水溶液的溶质质量分数,取该过氧化氢溶液68.0g放入烧杯中然后称量得到108.8g,然后加入2.0g二氧化锰,完全反应后,再称量其质量为110.0g。请回答下列问题:
①生成的氧气为_____g;蒸干烧杯内液体,所得固体物质为_____g。
②试通过计算求该过氧化氢溶液中溶质的质量分数。_____(要有计算过程,结果精确到0.1%)











