-
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2.则:
(1)D的元素符号为___________,A的单质分子中π键的个数为___________;
(2)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是
(3)A、B、C 3种元素的第一电离能由大到小的顺序为___________(用元素符号表示);
(4)写出基态E原子的价电子排布式___________。
-
(化学——选修3:物质结构与性质)
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是__________________。
(2)A、B、C 三种元素的氢化物稳定性由强到弱的顺序为_________(用化学式表示)。
(3)A的最简单氢化物分子的空间构型为_______,其中A原子的杂化类型是________。
(4)A的单质中δ键的个数为_______________,π键的个数为_______________。
(5)写出基态E原子的价电子排布式:__________________________。
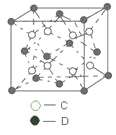
(6)C和D形成的化合物的晶胞结构如图所示,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a =________cm。(用ρ、NA的计算式表示)
-
(15分)有A、B、C、D、E五种原子序数均小于30且依次增大的元素。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)C、D形成的化合物化学式为______,A的单质分子中π键的个数为________。
(2)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是_____________。
(3)A、B、C三种元素的第一电离能由大到小的顺序为______(用元素符号表示)。
(4)向E单质与适量浓硫酸反应后的溶液中逐滴加入A的最简单气态氢化物的水溶液,看到的现象是____________。
(5)A的最简单氢化物分子易与H+结合生成空间正四面体形的阳离子,而A与C形成的分子却难与H+结合,原因是_____________。
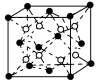
(6)C和D形成的化合物的晶胞结构如上图所示,已知晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,则晶胞边长a=________cm(用ρ、NA的计算式表示) 。
-
有A,B,C,D,E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)D的元素符号为______。A的单质分子中π键的个数为______。
(2)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是__________________________________。
(3)A,B,C 3种元素的第一电离能由大到小的顺序为________(用元素符号表示)。
(4)写出基态E原子的价电子排布式:__________________。
(5)A的最简单氢化物分子的空间构型为________,其中A原子的杂化类型是________。
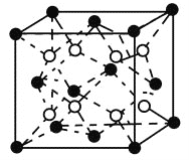
(6)C和D形成的化合物的晶胞结构如图所示,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a=________cm。(用ρ、NA的计算式表示)
-
有A,B,C,D,E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)D的元素符号为______。A的单质分子中π键的个数为______。
(2)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是__________________________________。
(3)A,B,C 3种元素的第一电离能由大到小的顺序为________(用元素符号表示)。
(4)写出基态E原子的价电子排布式:__________________。
(5)A的最简单氢化物分子的空间构型为________,其中A原子的杂化类型是________。
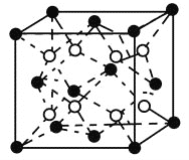
(6)C和D形成的化合物的晶胞结构如图所示,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a=________cm。(用ρ、NA的计算式表示)
-
有A,B,C,D,E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)D的元素符号为______。A的单质分子中π键的个数为______。
(2)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是__________________________________。
(3)A,B,C 3种元素的第一电离能由大到小的顺序为________(用元素符号表示)。
(4)写出基态E原子的价电子排布式:__________________。
(5)A的最简单氢化物分子的空间构型为________,其中A原子的杂化类型是________。
(6)C和D形成的化合物的晶胞结构如图所示,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a=________cm。(用ρ、NA的计算式表示)
-
有A,B,C,D,E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)D的元素符号为______。A的单质分子中π键的个数为______。
(2)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是__________________________________。
(3)A,B,C 3种元素的第一电离能由大到小的顺序为________(用元素符号表示)。
(4)写出基态E原子的价电子排布式:__________________。
(5)A的最简单氢化物分子的空间构型为________,其中A原子的杂化类型是________。
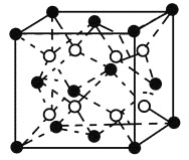
(6)C和D形成的化合物的晶胞结构如图所示,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a=________cm。(用ρ、NA的计算式表示)

-
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E的内部各能层均排满,且最外层有一个电子;D与E同周期,价电子数为2。则:
(1)写出基态E原子的价电子排布式___________。
(2)A的单质分子中π键的个数为________。
(3)A、B、C三种元素第一电离能由大到小的顺序为_______(用元素符号表示)
(4)B元素的氢化物的沸点是同族元素中最高的,原因是_______。
(5)A的最简单氢化物分子的空间构型为_____,其中A原子的杂化类型是__。
(6)C和D形成的化合物的晶胞结构如图,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a=__________ pm. (用ρ、NA,C和D化合物的摩尔质量为M g.mol-1的计算式表示)

-
有A、B、C、D、E、F六种原子序数依次增大的元素(原子序数均小于36)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E的d能级有一对成对电子;D元素与E同周期,价电子数为2;F元素与B同主族。则:
(1)写出与F元素同族,比F元素多两个周期的元素的基态原子的价电子排布图______________,A的单质分子的结构式为______________。
(2)A元素的一种氢化物为A2H4,其中A原子的杂化类型是______________,A2H4的水溶液呈碱性,用离子方程式表示A2H4溶液呈碱性的原因_____________________。
(3)在测定C(字母)的氢化物的相对分子质量时,实验测得值一般高于理论值,其主要原因是______________________________。
(4)AB2-离子的空间构型为_______________,写出由短周期元素形成的两种与AB2-互为等电子体的分子的化学式___________、___________。
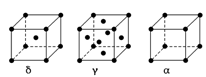
(5)E元素有δ、γ、α三种同素异形体,晶胞结构如右图所示。三种晶体的晶胞中所含有的E原子数之比为___________,若δ-Fe晶胞参数为apm,α-Fe晶胞参数为bpm,则两种晶体密度比为__________。
-
有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)由这五种元素组成的一种化合物是(写化学式)________________________。
(2)写出C元素基态原子的电子排布式_________________________。
(3)用轨道表示式表示D元素原子的价电子构型____________________。
(4)元素B与D的电负性的大小关系是___________,C与E的第一电离能的大小关系是___________。(填﹥、﹤、﹦,并且用元素符号表示)







