-
已知硫酸、氨水的密度与所加水量的关系如下图所示:
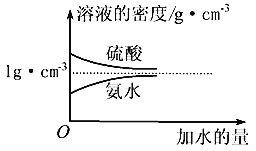
现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶液 | 溶质的物质的量浓度 | 溶液的密度/g·cm-3 |
| 硫酸 | 4 mol·L-1 | ρ1 |
| 2 mol·L-1 | ρ2 |
| 氨水 | 4 mol·L-1 | ρ3 |
| 2 mol·L-1 | ρ4 |
(1)ρ1、ρ2、ρ3、ρ4由大到小的顺序为:________。
(2)表中2 mol·L-1氨水的质量分数为:________。
(3)将4 mol·L-1的氨水与2 mol·L-1的硫酸等体积混合,所得溶液呈______性(填“酸”、“碱”、“中”);溶液中离子浓度从大到小的顺序是:__________________________。
(4)将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数是______。
A.>15% B.=15% C.<15% D.无法判断
(5)100g浓度为4 mol·L-1的硫酸溶液与_____mL水混合,可以使硫酸的物质的量浓度减小到2 mol·L-1。
-
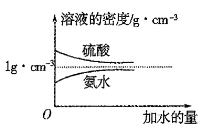
已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶质的物质的量浓度/mol· | 溶液的密度/g· |
| 硫酸 | 
| 
|
| 氨水 | 
| 
|
(1)表中硫酸的质量分数为 (用含 、
、 的代数式表示
的代数式表示 )。
)。
(2)物质的量浓度为 mol·
mol· 的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为
的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为  。
。
(3)物质的量浓度为 的氨水与
的氨水与 的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”下同)
的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”下同) ,所得溶液的物质的量浓度
,所得溶液的物质的量浓度  (设混合后溶液的体积变化忽略不计)。
(设混合后溶液的体积变化忽略不计)。
-
现有室温下溶质浓度均为 的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
(1)在④溶液中,各离子浓度大小顺序为:____________
(2)将③、⑥混合后,若溶液呈现中性,则消耗量溶液的体积为③____________⑥(填“>”、“=”或“<”),溶液中的离子浓度由大到小的顺序为____________
(3)在常温下,将100mL的②与100mL的⑥溶液混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=____________(已知 )
)
(4)在常温下,六种液体的pH由大到小的顺序是____________
(5)若将③溶液和⑥溶液按体积比2:1混合后溶液呈酸性,则混合后溶液中 __________
__________ (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
(6)常温下将③溶液加水稀释过程中,下列表达式的数据一定变大的是______
A、 B、
B、 C、
C、 D、
D、
-
现有室温下溶质浓度均为1×10﹣3 mol/L的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
(1)一水合氨的电离方程式为_______,硫酸铵在水溶液中水解的离子方程式为_______。
(2)将③、⑥混合后,若溶液呈中性,则消耗两溶液的体积为③________⑥(填“>”、“=”或“<”),溶液中的离子浓度由大到小的顺序为____________________________。
(3)在某温度下(Kw=1×10﹣12),将100 mL的①与100 mL的⑥溶液混合后(假设混合后溶液的体积为混合前两溶液的体积之和),溶液的pH=_________。
(4)若将等体积的②、③溶液加热至相同温度后,溶液的pH ②_______③(填“>” 、“=”或“<”)。
(5)若将③溶液和⑥溶液按体积比2:1混合后溶液呈酸性,则混合后溶液中c(CH3COO-)_______ c(CH3COOH)(填“>” 、“=”或“<”)
(6)室温时,若用①滴定⑤,适宜的指示剂为_____,当滴定过程中pH=9时,且溶液中满足4c(NH4+)=7c(NH3·H2O),则氨水的电离平衡常数Kb(NH3·H2O)=____(填数值)。
-
现有室温下溶质浓度均为 的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
(1)室温时,若用①滴定⑤,最佳的指示剂为____________,滴定终点时溶液呈____________性
(2)在④溶液中,各离子浓度大小顺序为:____________
(3)将③、⑥混合后,若溶液呈现中性,则消耗量溶液的体积为③____________⑥(填“>”、“=”或“<”),溶液中的离子浓度由大到小的顺序为____________
(4)在常温下,将 的②与
的②与 的⑥溶液混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的
的⑥溶液混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的 ____________(已知
____________(已知 )
)
(5)在常温下,六种液体的 由大到小的顺序是____________
由大到小的顺序是____________
(6)若将③溶液和⑥溶液按体积比2:1混合后溶液呈酸性,则混合后溶液中 ____________
____________ (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
(7)常温下将③溶液加水稀释过程中,下列表达式的数据一定变大的是____________
A、 B、
B、 C、
C、 D、
D、
-
Cu可形成多种配合物,某同学在探究配合物的形成时做了以下实验,根据下列信息回答问题:
(1)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,请写出先后发生反应的离子方程式___________。
(2)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为__________________。
(3)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3________(填“>”“=”或“<”)H2O。
(4)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一种为绿色。两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,某同学设计了如下实验:
a、分别取等质量的两种配合物晶体的样品配成待测溶液;
b、分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c、沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的 。绿色晶体配合物的化学式为____________,由Cl所形成的化学键类型是_____________。
。绿色晶体配合物的化学式为____________,由Cl所形成的化学键类型是_____________。
-
(1)现有下列物质①NaCl晶体 ②液态SO2 ③纯醋酸 ④硫酸钡 ⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KNO3 ⑧NaOH溶液 ⑨氨水 请用以上物质回答下列问题(填序号)。
在上述状态下能导电的强电解质是__________________; 属于弱电解质的是________________;属于非电解质,但溶于水后的水溶液能导电的是_________________。
(2)化学平衡移动原理同样也适用于其他平衡,已知在氨水中存在下列平衡:NH3·H2O  NH4++OH-。
NH4++OH-。
①向氨水中加入NH4Cl固体时,平衡____________移动,(填“向右”或“向左”),c(OH-)____(填“增大”或“减小”,下同),c(NH4+)______。
②向氨水中加入MgCl2固体时,平衡_____移动,(填“向右”或“向左”),c(OH-)____(填“增大”或“减小”,下同),c(NH4+)_________。
③升高温度,c(OH-)______(填“增大”或“减小”,下同),c(NH4+)___。
-
(1)现有下列物质 ①NaCl晶体 ②液态SO2 ③纯醋酸 ④硫酸钡⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KNO3 ⑧NaOH溶液 ⑨氨水 请用以上物质的序号回答下列问题:
属于强电解质的是________; 属于弱电解质的是_______;在上述状态下能导电的物质是_________。
(2)化学平衡移动原理同样也适用于其它平衡,已知在氨水中存在下列平衡:NH3·H2O  NH4++OH-
NH4++OH-
①向氨水中加入NH4Cl固体时,平衡____________移动,(填“向右”或“向左”),c(OH-)____(填“增大”或“减小”,下同)。
②向氨水中加入MgCl2固体时,平衡_____移动,(填“向右”或“向左”), c(NH4+)____(填“增大”或“减小”)
-
已知氨水的密度比水小,现有质量分数分别为10%利50%的两种氨水,将其等体积混合,则所得混合溶液溶质质量分数是
A. >30% B. =30% C. <30% D. 无法确定
-
已知氨水的密度比水小,现有质量分数分别为10%利50%的两种氨水,将其等体积混合,则所得混合溶液溶质质量分数是
A. >30% B. =30% C. <30% D. 无法确定

