-
甲、乙、丙、丁、戊五种元素,其中甲元素原子核外L层上s能级和p能级电子个数相同;乙元素原子3p能级上只有1对成对电子;丙和丁元素原子N层上都只有1个电子,但其中丙元素原子各内层均已充满;而丁元素原子次外层的电子充满在2个能级中;戊元素原子最外层电子排布图是
,它的单质常温时为气态。试用化学符号回答以下问题。
(1)甲是___,乙是___,丙是___,丁是___,戊是__。
(2)丙和乙的单质发生化合反应的化学方程式是:___。
(3)丙的硝酸盐溶液跟乙的气态氢化物发生反应的离子方程式是:___。
(4)甲和乙元素组成的化合物的化学式是___,用电子式表示该化合物的形成过程___。
(5)乙和戊元素的气态氢化物沸点高低关系是___>___。
(6)丙的硫酸盐跟少量氨水反应的离子方程式是:___。
(7)丙元素原子的外围电子排布式是___。
(8)乙和丁形成的化合物的电子式是___。
高二化学推断题中等难度题查看答案及解析
-
下列关于主族元素电了排布特征的说法正确的是
A.主族元素的原子核外电子最后填入的能级是s能级
B.主族元素的原子核外电子最后填入的能级是s能级或p能级
C.主族元素的原子核外电子最后填入的能级是d能级或f能级
D.主族元素的原子核外电子最后填入的能级是s能级或d能级
高二化学选择题中等难度题查看答案及解析
-
现有部分短周期元素的性质或原子结构如下表:
元素
元素性质或原子的结构
T
2p轨道能级电子数比s能级电子数多1个
X
L层p能级电子数比s能级电子数多2个
Y
第三周期元素的简单离子中半径最小
Z
L层有3个未成对电子
(1)写出元素X的离子结构示意图: .写出元素Z的简单气态氢化物的电子式: .
(2)写出元素Y的最高价氧化物对应的水化物与KOH反应的化学方程式: .
(3)T、Y、Z三种元素的单质中化学性质明显不同于其他单质的是 (填元素符号,下同);元素T与氯化素相比,非金属性较强的是 ,下列表述中能证明这一事实的是 (填字母).
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液中不能置换出来
c.氯与T形成化合物中,氯元素呈正价.
高二化学填空题简单题查看答案及解析
-
下列关于主族元素的说法正确的是
A.主族元素的原子核外电子最后填入的能级是s能级
B.主族元素的原子核外电子最后填入的能级是s能级或p能级
C.主族元素的价电子数有可能超过最外层电子数
D.主族元素的最高正价一般等于该元素所在主族的族序数
高二化学选择题中等难度题查看答案及解析
-
下列关于主族元素的说法正确的是( )
A.主族元素的原子核外电子最后填入的能级是s能级
B.主族元素的原子核外电子最后填入的能级是s能级或p能级
C.主族元素的最高正价一定等于主族的序数
D.主族元素的价电子数有可能超过最外层电子数高二化学选择题中等难度题查看答案及解析
-
下列关于主族元素的说法正确的是( )
A.主族元素的原子核外电子最后填入的能级是s能级
B.主族元素的原子核外电子最后填入的能级是s能级或p能级
C.所有主族元素的最高正价都等于主族序数
D.主族元素的价电子数有可能超过最外层电子数
高二化学单选题简单题查看答案及解析
-
A、B、C、D、E、F、G七种元素,它们的原子序数依次增大,除G外均为前20号元素。A原子基态时p能级原子轨道上电子数等于次外能层电子数,C元素的原子基态时s能级与p能级上的电子数相等,C、D处于相同的能级,且D是同期中电负性最大的元素,E原子的第一至第四电离能(kJ·mol-1)分别为:578、1817、2745、11575,F元素原子中4s能级有2个电子。G元素的离子形成的硫酸盐结晶水合物呈蓝色。
(1)B形成的单质中σ键和Π键的个数比为________,上述元素形成的化合物中和B的单质是等电子体的是__________(填化学式)
(2)G元素的基态原子的电子排布式为 。
(3)常温下,E单质投入到B的最高价氧化物对应的水化物的浓溶液中的现象是 。
(4)D、F组成的晶体FD2结构如图Ⅰ所示,G形成晶体的结构如Ⅲ所示,Ⅱ为H3BO3(硼酸)晶体结构图(层状结构,层内的H3BO3分子通过氢键结合)。
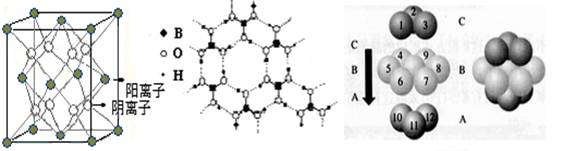
图Ⅰ 图Ⅱ 图Ⅲ
①图Ⅰ所示的FD2晶体中与F离子最近且等距离的F离子数为________,图Ⅲ中未标号的G原子形成晶体后周围最紧邻的G原子数为________;
②图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是(写元素符号),H3BO3晶体中B原子个数与极性键个数比为________;
③三种晶体中熔点高低的顺序为________ ________(填化学式),H3BO3晶体受热熔化时,克服的微粒之间的相互作用为________。
高二化学填空题极难题查看答案及解析
-
有A、B、C、D、E、F六种原子序数依次增大的元素(原子序数均小于36)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E的d能级有一对成对电子;D元素与E同周期,价电子数为2;F元素与B同主族。则:
(1)写出与F元素同族,比F元素多两个周期的元素的基态原子的价电子排布图______________,A的单质分子的结构式为______________。
(2)A元素的一种氢化物为A2H4,其中A原子的杂化类型是______________,A2H4的水溶液呈碱性,用离子方程式表示A2H4溶液呈碱性的原因_____________________。
(3)在测定C(字母)的氢化物的相对分子质量时,实验测得值一般高于理论值,其主要原因是______________________________。
(4)AB2-离子的空间构型为_______________,写出由短周期元素形成的两种与AB2-互为等电子体的分子的化学式___________、___________。
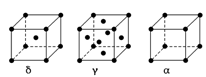
(5)E元素有δ、γ、α三种同素异形体,晶胞结构如右图所示。三种晶体的晶胞中所含有的E原子数之比为___________,若δ-Fe晶胞参数为apm,α-Fe晶胞参数为bpm,则两种晶体密度比为__________。
高二化学填空题困难题查看答案及解析
-
Q、T、X、Y、Z、W六种元素为前四周期原子序数依次增大的元系,其中Q元素的氢化物的水溶液pH>7;元素X、Y位于同一主族,元素X基态原子核外电子处于三个不同的能级,且s能级的电子总数比p 能级的电子总数少1。元素Z位于IVB,元素W的基态原子内层电子全充满,最外层电子数为3。(请用对应的元素符号回答相关问题)
(1)写出W的基态原子的价电子排布式: _________.
(2)Q、T、X的第一电离能由大到小的顺序为__________________。
(3)化合物Y2T的空间构型为_________,中心原子的价层电了对数为___________单质Y与湿润的Na2CO3 反应可制备Y2T,其化学方程式为_________。
(4)Q的氢化物极易溶于水,其主要原因是_________。
(5)已知Z3+可形成配位数为6的配合物。现有含2的两种颜色的晶体,一种为紫色,另一种为绿色,但相关实验证明,两种品体的组成皆为ZCl3•6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的2/3。则绿色晶体配合物的化学式为_______。
高二化学综合题中等难度题查看答案及解析
-
X、Y、Z、M、W是原子序数依次增大的前四周期元素,X元素原子核外有三个能级,各能级电子数相等,Y的单质在空气中燃烧生成一种淡黄色的固体;Z元素原子的最外层电子数比次外层电子数少2,M原子外围电子排布式为3dn4sn;W的内层电子已全充满,最外层只有2个电子。
请回答下列问题:
(1)X元素在周期表中的位置是____;W2+离子的外围电子排布式为___。
(2)X 能与氢、氮、氧三种元素构成化合物 XO(NH2)2,其中X原子和N原子的杂化方式为分别为___、___,该化合物分子中的π键与σ键的个数之比是____;该物质易溶于水的主要原因是___。
(3)已知Be和Al元素处于周期表中对角线位置,化学性质相似,请写出Y元素与Be元素两者相应的最高价氧化物对应水化物相互反应的化学方程式:____。
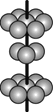
(4)M晶体的原子堆积方式为六方堆积(如图所示),则晶体中M原子的配位数是___。某M配合物的化学式是[M(H2O)5Cl]Cl2·H2O,1 mol该配合物中含配位键的数目是____。
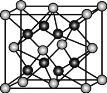
(5)Y离子和Z离子比较,半径较大的是___(填离子符号),元素Y与元素Z形成的晶体的晶胞结构是如图所示的正方体,每个Y离子周围与它最近的Y离子有___个。
高二化学填空题中等难度题查看答案及解析